硫酸铜的制备
目的原理
实验目的
1.练习和掌握加热、蒸发浓缩,常压过滤及减压过滤,重结晶等基本操作;
2.了解由金属与酸作用制备盐的方法。
实验原理
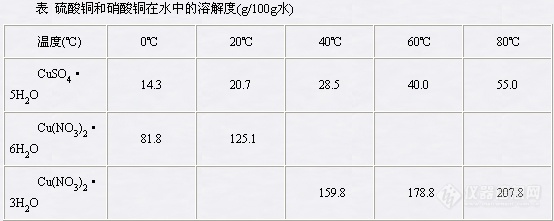
纯铜不活泼,不能溶于非氧化性的酸中。但其氧化物在稀酸中却极易溶解。因此在工业上制备胆矾时,先把铜烧成氧化铜,然后与适当浓度的硫酸作用生成硫酸铜。本实验采用浓硝酸作氧化剂,以铜片与硫酸、浓硝酸作用来制备硫酸铜。溶液中生成硫酸铜外,还含有一定量的硝酸铜和其他一些可溶性或不溶性的杂质。不溶性杂质可过滤除去。利用硫酸铜和硝酸铜在水中溶解度的不同可将硫酸铜分离、提纯。
![]()
由上表中数据可见,硝酸铜在水中的溶解度不论在高温或低温下都比硫酸铜大得多。因此,当热溶液冷却到一定温度时,硫酸铜首先达到过饱和而开始从溶液中结晶析出,随着温度的继续下降,硫酸铜不断从溶液中析出,硝酸铜则大部分仍留在溶液中,只有小部分随着硫酸铜析出。这小部分硝酸铜的其他一些可溶性杂质,可再经重结晶的方法而被除去,最后达到制得纯硫酸铜的目的。
过程步骤
一、铜片的净化
称取4.5g剪细的铜片,放在蒸发皿中,加入10ml mol·dm-33,在小火上微热,以洗去铜片上的污物(注意不要加热太久,以免使铜过多地溶解在稀HNO3中,影响产率)。用倾析法除去酸液,并用水洗净铜片。
如果用废铜屑为原料,应先放在蒸发皿中,以强火灼烧,至表面生成黑色CuO为止,自然冷却,再作粗CuSO4·5H2O的制备。
二、五水硫酸铜的制备
在通风柜中,往盛有铜片的蒸发皿中加入15ml 3mol·dm-3H2SO4,然后慢慢分批加入7ml浓硝酸组成的混酸(此过程应根据反应情况的不同而决定补加混酸的量)。待反应完全后(铜片近于全部溶解),趁热用倾析法将溶液转至一个小烧杯中,留下不溶性杂质,然后再将硫酸铜溶液转回到洗净的蒸发皿中,在水浴上缓慢加热,浓缩至表面有晶体膜出现为止。取下蒸发皿,使溶液逐渐冷却,析出蓝色的CuSO4·5H2O晶体。抽滤、称重。计算产率(以湿品计算,应不少于85%)。
产品重量 g
理论产量 g
产率 %
三、重结晶法提纯五水硫酸铜
将上面制得粗CuSO4·5H2O晶体在台称上称出1g留作分析用,其余放在小烧杯中,按重量比CuSO4·5H2O∶H2O = 1∶3的比例加入纯水,加热搅拌,促使溶解。滴加2ml3%H2O2,将溶液加热,同时逐滴加入2mol·dm-3氨水(或0.5mol·dm-3NaOH)直到溶液pH = 4,再多滴1-2滴,加热片刻,静置使水解产物的Fe(OH)3沉降。用倾析法在普通漏斗上过滤,滤液流入洁净的蒸发皿中。在提纯后的滤液中,滴加1mol·dm-3H2SO4酸化,调节pH至1-2,然后在石棉网上加热、蒸发、浓缩至液面出现一层结晶膜时,即停止加热。以冷水冷却,结晶抽滤,取出结晶,放在两层滤纸中间挤压,以吸干水份,称量。计算产率。
产品重量 g
理论产量 g
产品产率 %
四、产品纯度检验