10.钢铁表面一旦具备了形成腐蚀电池的条件,腐蚀就持续进行下去,是这样吗?
钢铁表面一旦具备了形成腐蚀电池的条件,腐蚀变会发生和发展,但发展速度还要取决于其他条件。为说明问题,还是以“干电池”作为例子。我们知道, “干电池”是典型的腐蚀电池,它伴随着阳极(锌皮)的腐蚀而提供电流。而电流的大小就代表腐蚀速度的大小。
当“干电池”用了一段时间之后,会发现电压不到原来的 1.5V 了,所提供的电流也会变小了。到后来锌皮锈穿(阳极面积变小) ,电流、电压都会降低,腐蚀速度就降下来。当达不到使用要求时,该电池就废弃了。
我们要问,为什么电压(电流)会降低?这里需要引出“极化”和“去极化”的概念,它们在解释腐蚀的运行、发展和腐蚀速度等方面是必不可少的。我们知道“干电池”中心的碳棒只是起导电作用,真正的“阴极”是碳棒周围所填充的“氧化剂” ,是它不断夺取由阳极(锌腐蚀)所传递过来的电子(还原反应) ,使两极之间保持 1.5V 的电位差(电压) 。需知,氧化剂是有一定数量的,当它消耗的一定程度,它不断夺取电子、还原反应的速度就慢下来,电子不能及时取走,就在阴极发生“积累” ,其结果使阴极电位负向变化、阴阳极之间的电位差(电压)变小(比如由原来的 1.5V 减少到 1.2V 了) 。当氧化剂全部耗尽是,阴阳极之间的电位差也不存在了,这个腐蚀电池便“寿终” 。使阴极还原反应受阻、迫使阴极电位负向变化的现象,称作“阴极极化” ;同理,阳极面积变小,回使阳极反应变得困难,还有一些其他因素会促使阳极氧化反应受阻、迫使阳极电位正向变化,这种现象,称作“阳极极化” 。可以看出,不论阴极极化还是阳极极化,都能使腐蚀电池的电位差缩小,使腐蚀速度放慢或终止。从减少腐蚀危害的观点看,极化现象是有利的,或者说是可以利用的思路与方法。所谓“去极化”就是不使其发生“极化”现象,比如在阴极有不断补充的氧化剂。
通常的氧气就是起到阴极“去极化”作用,因此氧是促进腐蚀电池不断运行、加速腐蚀的物质。
除了“极化”因素外,腐蚀电池阴极与阳极之间的电阻,也是控制腐蚀速度的重要因素。 通常钢铁表面要用涂层保护, 一方面是为了隔离环境, 使钢铁表面不能形成腐蚀电池 (完全做到是困难的) ,另一方面,就是加大阴极与阳极之间的电阻,最大限度地降低钢铁表面的腐蚀速度。
如前面已经阐明过,在自然环境中,钢铁腐蚀是“自发”的,完全阻止钢铁腐蚀是困难的。然而,依据腐蚀原理,最大限度地降低其腐蚀速度,是可以做到的,从而达到延长钢铁使用寿命的目的。
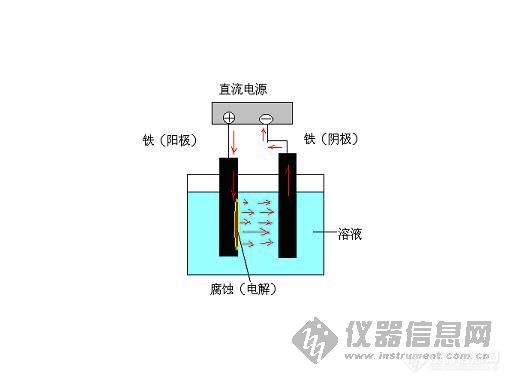
钢铁腐蚀有多个控制因素,这对于认识和理解防腐蚀原理来说,是非常重要的。每一个图 11-1“电解电池”示意图。
![]()
图 11-1 所示“电解电池”中,如果溶液是中性水,那么,电化学反应是:
阳极反应(氧化反应)式为:
Fe - 2e = Fe ++ (11-1)
阴极反应(还原反应)的表达式是:
2O2 + H2O + 4e = 4 OH - (11-2)
综合电化学过程(氧化还原反应) :
2Fe +O2 +2 H2O = 2Fe (OH)2 (11-3)
如果电解液中含有足够量的铜离子,那么,阴极反应会变为:
Cu++ + 2e = Cu (11-4)
作为阴极的铁棒表面回沉积一层铜,这正是电镀铜的原理,也是其他金属镀层生成的基本原理。电镀是钢铁防护的有效方法之一。