维权声明:本文为Insm_33d3dbf9原创作品,本作者与仪器信息网是该作品合法使用者,该作品暂不对外授权转载。其他任何网站、组织、单位或个人等将该作品在本站以外的任何媒体任何形式出现均属侵权违法行为,我们将追究法律责任。
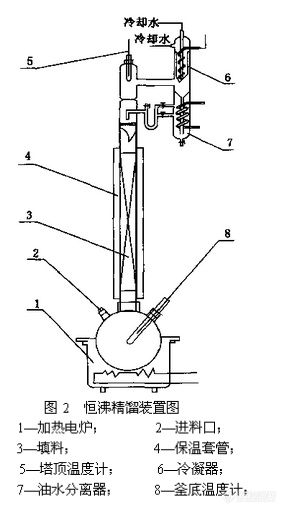
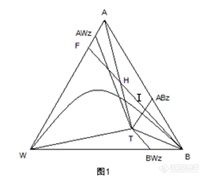
乙醇-水均相恒沸精馏实验实验目的精馏是利用不同组份在气-液两相间的分配,通过多次气液两相间的传质和传热来达到分离的目的。对于不同的分离对象,精馏方法也会有所差异。例如,分离乙醇和水的二元物系。由于乙醇和水可以形成共沸物,而且常压下的共沸温度和乙醇的沸点温度极为相近,所以采用普通精馏方法只能得到乙醇和水的混合物,而无法得到无水乙醇。为此,在乙醇-水系统中加入第三种物质,该物质被称为恒沸剂。恒沸剂具有能和被分离系统中的一种或几种物质形成最低共沸物的特性。在精馏过程中恒沸剂将以共沸物的形式从塔顶蒸出,塔釜则得到无水乙醇。这种方法就称作恒沸精馏(共沸精馏)。对此我们进行实验,以下为此实验的目的:加强并巩固对恒沸精馏过程的理解,了解乙醇和水的分离方法;能够对精馏过程做全塔物料衡算;熟悉实验室的精馏设备的构造,掌握精馏操作的方法;学会使用气相色谱分析气、液两相组成。二、实验原理 恒沸精馏是向恒沸溶液中加入第三组分,使该组分能与原有溶液中的一个或多个组分形成恒沸物,且这种新恒沸物的挥发度显著地高于或低于原有各组分的挥发度,则新恒沸物中各组分的含量与原料液组成不同,可采用普通精馏方法予以分离。分离二元均相恒沸物常用的方法是通过加入一种恒沸剂,使其改变原混合物的性质,再进行三元物系的分离。在常压下,用常规精馏方法分离乙醇-水溶液,最高只能得到浓度为95.57%的乙醇。这是乙醇与水形成恒沸物的缘故,其恒沸点78.15℃,与乙醇沸点78.30℃十分接近,形成的是均相最低恒沸物。而浓度95%左右的乙醇常称工业乙醇。 实验室中恒沸精馏过程的研究包括以下几个内容: 1.恒沸剂的选择 恒沸剂的选择对恒沸精馏分离过程的效果影响极大。选择恒沸剂,首先要考虑恒沸剂的选择性要大。此外,还应考虑以下几个方面: (1) 恒沸剂能显著影响待分离系统中关键组分的汽液平衡关系。 (2) 恒沸剂至少与待分离系统中一个或两个( 关键) 组分形成两元或三元最低恒沸物,而且希望此恒沸物比待分离系统中各纯组分的沸点或原来的恒沸点低10℃以上,否则难以实现精馏分离。 (3) 为使分离流程比较简单,恒沸剂回收容易,选用能生成均相恒沸物的恒沸剂。 (4) 在所形成的恒沸物中,恒沸剂的比例愈少愈好,汽化潜热愈小愈好。这样不仅可减少恒沸剂用量,提高恒沸剂效率; 也可减少循环量,以降低蒸发所需的热量及冷凝所需冷却的量。 (5) 恒沸剂易于回收利用。一方面希望形成均相恒沸物,可以减少分离恒沸物的操作; 另一方面,在溶剂回收塔中,应该与其它物料有相当大的挥发度差异。 (6) 恒沸剂廉价、来源广、无毒性、热稳定性好和腐蚀性小等。就工业乙醇制备无水乙醇,适用的恒沸剂有苯、正己烷、环己烷、乙酸乙酯等.它们都能与水-乙醇形成多种恒沸物,而且其中的三元恒沸物在室温下又可以分为两相,一相富含恒沸剂,另一相中富含水,前者可以循环使用,后者又很容易分离出来,这样使得整个分离过程大为简化,对于本实验我们采用正己烷作为恒沸剂。 2.三相图三组分纯物质及恒沸物沸点图,并在三角形相图中给出三组分恒沸物溶解度曲线 图1 恒沸精馏原理图 3.恒沸剂的加入方式恒沸剂一般可随原料一起加入精馏塔中,若恒沸剂的挥发度比较低,则应在加料板的上部加入,若恒沸剂的挥发度比较高,则应在加料板的下部加入。目的是保证全塔各板上均有足够的恒沸剂浓度。 4.恒沸剂用量的确定 恒沸剂理论用量的计算可利用三角形相图按物料平衡式求解。若原溶液的组成为F点,加入恒沸剂S以后,物系的总组成将沿FB线向着B点移动。当物系的总组成移到G点时,恰好能将水以三元恒沸物的形式带出,以单位原料液F为基准,对水作物料衡算,得, 恒沸剂S的理论用量为: 式中:F—进料量; D—塔顶三元恒沸物量; S—恒沸剂理论用量;Xf,i—组分的原料组成; XD,i—塔顶恒沸物中i组成。5.流程图三、实验装置与试剂1.实验装置 实验所用的精馏柱为内径20mm的玻璃塔,塔内分别装有不锈钢三角形填料和压延孔环填料,填料层高1m。塔身采用真空夹套以便保温。塔釜为100ml的三口烧瓶,其中位于中间的一个口与塔身相连,侧面的一开口为测温口,用于测量塔釜液相温度,另一开口作为进料和取样口。塔釜配有350W电热器,加热并控制釜温。 经加热沸腾后的蒸汽通过填料层到达塔顶,塔顶采用一特殊冷凝头,以满足不同操作方式的需要。既可实现连续精馏操作,又可进行间歇精馏操作。塔顶冷凝液流入分层器后,分为两相,上层为油相,下层含水。![]() 图2 恒温精馏装置图 2.试剂 乙醇(95%),正己烷,气相色谱仪四、实验步骤 1.称取X克95%(质量分数)乙醇,按恒沸剂的理论用量算出加入量; 2.将配置好的原料加入塔釜中,开启塔釜,加热电源及塔顶冷却水; 3.当塔顶有冷凝液时,便要注意调节回流流量,实验过程采用油相回流; 4.每隔10分钟记录一次塔顶塔釜温度,每隔20分钟,取塔釜液相样品分析,当塔釜温度升到80℃时,若釜液纯度达98.37%以上即可停止实验; 5.取出分相器中的富水层,称重并进行分析。 6.切断电源,关闭冷却水,结束实验;7.实验中各点的组成均采用气相色谱仪分析法分析。五、实验数据记录
图2 恒温精馏装置图 2.试剂 乙醇(95%),正己烷,气相色谱仪四、实验步骤 1.称取X克95%(质量分数)乙醇,按恒沸剂的理论用量算出加入量; 2.将配置好的原料加入塔釜中,开启塔釜,加热电源及塔顶冷却水; 3.当塔顶有冷凝液时,便要注意调节回流流量,实验过程采用油相回流; 4.每隔10分钟记录一次塔顶塔釜温度,每隔20分钟,取塔釜液相样品分析,当塔釜温度升到80℃时,若釜液纯度达98.37%以上即可停止实验; 5.取出分相器中的富水层,称重并进行分析。 6.切断电源,关闭冷却水,结束实验;7.实验中各点的组成均采用气相色谱仪分析法分析。五、实验数据记录表一、温度及塔釜组成随时间的变化关系数据表
时间/min | 塔顶温度 ℃ | 塔釜温度 ℃ | 釜液组成/xw% |
乙醇 | 水 | 正己烷 |
10 | | | | | |
20 | | | | | |
30 | | | | | |
40 | | | | | |
… | | | | | |
表二、气相色谱仪实验数据分析采集表
物相名称 | 质量/g | 物质 | 峰面积 | 质量矫正因子 | 质量分数 | 质量/g |
富水相 | | 水 | | | | |
乙醇 | | | | |
正己烷 | | | | |
富正己烷相 | | 水 | | | | |
乙醇 | | | | |
正己烷 | | | | |
塔釜 | | 水 | | | | |
乙醇 | | | | |
正己烷 | | | | |
原料乙醇 | | 水 | | | | |
乙醇 | | | | |
| 水 | | | | |
乙醇 | | | | |
原料正己烷 | | 正己烷 | | | | |
六、计算实例以以下这组数据为例进行计算:物系 | 进料量kmol/h | 进料组成xf | 塔釜组成xw |
乙醇—水 | 100 | 0.38 | 0.99 |
计算恒沸剂的质量流量 解:由题意得F:100 Kmol/h XF:0.38 Xw:0.99七、实验结果及讨论 ![]() 八、预习与思考1、如何计算连续精馏中恒沸剂的最小加入量? 答:⑴在指定的压力下,做水-乙醇-正己烷的三角相图;⑵根据相关文献在图上确定共沸物组成点(自由度为1,所以务必确定是该压力下的共沸点组成),包括三元恒沸物,所有可能的二元恒沸物。按照实验原理中的说明做出下面的连线。由沸点参数可知,原料液组成应控制在ΔATABZ中;⑶连接F,B两点,交ΔATABZ于H和I,这两点分别是加入恒沸剂的最小量和最大量。⑷从图上可以读出各线段长度。利用杠杆规则,恒沸剂最小加入量时混合液的组成为H, 则mB=mF*|HF|/|BH|。2、分析实验过程中产生误差的原因?答:之所以会引起误差,主要是因为该求算方法计算的只是塔顶馏出液的组成,而塔顶馏出液实际上是三元恒沸物与二元恒沸物的混合液。该实验过程并没有很好地对三元恒沸物蒸尽的临界点进行控制,因而没法按照精确方法计算。3、除无水乙醇恒沸剂外,查文献说明,还有哪些物系,可以用恒沸精馏方法分离?答: 在文献中,分别用苯、环己烷、正己烷、乙酸乙酯、三氯甲烷为恒沸剂,恒沸精馏135min,结果如下表:
八、预习与思考1、如何计算连续精馏中恒沸剂的最小加入量? 答:⑴在指定的压力下,做水-乙醇-正己烷的三角相图;⑵根据相关文献在图上确定共沸物组成点(自由度为1,所以务必确定是该压力下的共沸点组成),包括三元恒沸物,所有可能的二元恒沸物。按照实验原理中的说明做出下面的连线。由沸点参数可知,原料液组成应控制在ΔATABZ中;⑶连接F,B两点,交ΔATABZ于H和I,这两点分别是加入恒沸剂的最小量和最大量。⑷从图上可以读出各线段长度。利用杠杆规则,恒沸剂最小加入量时混合液的组成为H, 则mB=mF*|HF|/|BH|。2、分析实验过程中产生误差的原因?答:之所以会引起误差,主要是因为该求算方法计算的只是塔顶馏出液的组成,而塔顶馏出液实际上是三元恒沸物与二元恒沸物的混合液。该实验过程并没有很好地对三元恒沸物蒸尽的临界点进行控制,因而没法按照精确方法计算。3、除无水乙醇恒沸剂外,查文献说明,还有哪些物系,可以用恒沸精馏方法分离?答: 在文献中,分别用苯、环己烷、正己烷、乙酸乙酯、三氯甲烷为恒沸剂,恒沸精馏135min,结果如下表:表三、恒沸剂类型与塔釜乙醇浓度关系
恒沸剂 | 苯 | 环己烷 | 正己烷 | 乙酸乙酯 | 三氯甲烷 |
乙醇浓度/% | 99.25 | 99.88 | 98.37 | 98.61 | 99.45 |
由表1可以看出,使用环己烷作为恒沸剂,制备无水乙醇的效果最佳,可得到99. 88% (质量分率)的无水乙醇。可达到同样效果的恒沸剂还有苯和CHCl3,然而苯的毒性太大,对环境的污染比较严重;CHCl3 的理论加入量远大于环己烷,浪费原料。4、均相和非均相连续恒沸精馏的共同点和区别是什么?试分别阐述。 答:区别:非均相恒沸精馏中加入第三组分(恒沸剂)后能与原来的组分形成两个液相,采用分相器使恒沸剂回流,另一相采出,可以节省恒沸剂的使用量;而均相恒沸精馏回流到塔内的是多组元恒沸物,恒沸剂的用量和能耗均较高。 共同点:均是通过加入恒沸剂与系统中一种或多种物质形成最低恒沸物,恒沸剂以恒沸物的形式从塔顶蒸出,塔釜得到相对较纯的组分。


 八、预习与思考
八、预习与思考