维权声明:本文为nphfm2009原创作品,本作者与仪器信息网是该作品合法使用者,该作品暂不对外授权转载。其他任何网站、组织、单位或个人等将该作品在本站以外的任何媒体任何形式出现均属侵权违法行为,我们将追究法律责任。
化学试剂与工业产品氟化氢铵含量的测定差别
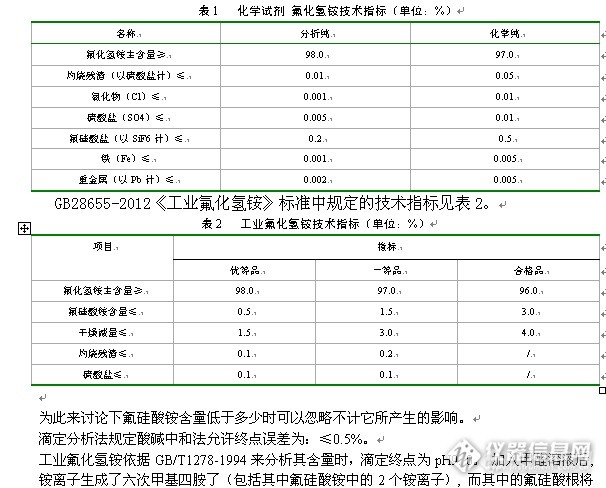
摘要 本文从滴定分析原理、指示剂的选择详细讲述了化学试剂与工业产品氟化氢铵含量的分析方法差别,其差别的原因主要在于工业产品氟化氢铵中所含有的氟硅酸,并指出当工业产品氟化氢铵中的氟硅酸铵含量低于0.5%时,两个滴定方法才可以互相通用的。关键词 化学试剂氟化氢铵;工业产品氟化氢铵;滴定分析;分析方法差别;氟硅酸;1 引言化学试剂氟化氢铵与工业产品氟化氢铵的生产企业均列入了工业产品生产许可管理范围,但企业实地核查过程中发现,不少的工业产品氟化氢铵的生产企业检验人员在分析氟化氢铵主含量时所采用的滴定方法与化学试剂氟化氢铵的滴定方法是一样的,为此写本文以对两者的滴定方法的差异作一解释。2 材料与试剂甲醛液(1+1
);酚酞指示剂(10g/L
);硝酸钾饱和液;溴百里酚蓝(0.5g/L
)-中性红混合指示液(0.5g/L
)(1+1
);碎冰;0.5moL/L
氢氧化钠标准溶液;超纯水;50mL
碱式滴定管:A
级;电子分析天平:AL2104
(上海精密科学仪器有限公司产)3 实验方法3.1化学试剂氟化氢铵含量的滴定方法GB/T1278-1994《化学试剂氟化氢铵》[1]氟化氢铵含量的测定 称取0.8g
试样,精确至0.0001g
。置于塑料杯中,
加20mL
水溶解,
加40mL
已经预先中和至中性的甲醛液(1+1
),
摇匀,
放置30min
,加2
滴10g/L
酚酞指示液,
用0.5moL/L
的氢氧化钠标液滴定到溶液呈粉红色,
并保持5min
。 含量按下式计算: X =C
×V
×0.02852
×100/m
式中:X
—氟化氢铵的百分含量;%
V
—试样消耗氢氧化钠标准液的体积数;mL
C
—0.5moL/L
氢氧化钠标液的准确浓度,moL/L
0.02852
—氢氧化钠换算成氟化氢铵的系数,g/mmoL
m
—试样的质量,g
3.2 工业产品氟化氢铵含量的滴定方法GB28655-2012《工业氟化氢铵》[2]氟化氢铵含量的测定称取0.8g
试样,精确至0.0001g
。用少量冷水将试样转移至预先盛有20mL
硝酸钾饱和溶液和50g
碎冰的塑料烧杯中,并搅拌至试样溶解。加入5
滴溴百里酚蓝-中性红混合指示液,
用0.5moL/L
氢氧化钠标液滴定至样液呈深绿色为终点(pH7.2
)。含量按下式计算: X =C
×V
×0.05704
×100/m
式中:X
—氟化氢铵的百分含量,%
V
—试样消耗氢氧化钠标准液的体积数,mL
C
—0.5moL/L
氢氧化钠标液的准确浓度,moL/L
0.05704
—氢氧化钠换算成氟化氢铵的系数,g/mmoL
m
—试样的质量,g
4 结果与讨论比较这两个标准,很明显地看到:同样是分析氟化氢铵主含量,但滴定所用的指示剂,
方法原理却是不一样的。下面作一阐述:4.1 化学试剂氟化氢铵含量的测定其依据是甲醛法测定铵盐的通用方法4.1.1
原理:铵根与甲醛生成六次甲基四胺(也叫六亚甲基四胺),同时释放出氢离子,六次甲基四胺结合一个氢离子,转化成其盐,反应如下: NH
4HF
2 = HF + NH
4F
4NH
4+ + 6HCHO= (CH
2)
6N
4H
+ + 3H
+ + 6H
2O
H
+ + OH
- = NaOH
HF + NaOH = NaF + H
2O
质子化的六次甲基四胺(带1
个氢离子),因为酸性增强了,可以被氢氧化钠准确滴定,生成的另外三个氢离子实为强酸,中和时它们一起被同时滴定(四个铵根对应四个转化而来的氢离子,其中一个含在胺的共轭酸中)。关系:一个铵根对应一个氢离子,再对应一个氢氧化钠;而氟化氢铵可看成是NH4F
和HF
等比混合成的。故存在着这样的化学计量关系:NaOH :NH4HF2 = 2:1
可以推导出GB/T1278
公式中的计算系数:0.02852 g/mmoL
。4.1.2
指示剂的选择:指示剂选用酚酞。由于六次甲基四胺是极弱的有机碱,它的存在使等当点时溶液呈微碱性,又由于它是可逆反应,在酸性或中性溶液(pH
≤7.5
)中不能定量地完成(偏低);但是用氢氧化钠标准溶液滴定至终点pH9.0
时反应能进行到底,故选择酚酞指示液作为指示剂。4.2 工业产品氟化氢铵含量的测定当工业品氟化氢铵中的氟硅酸铵不能忽略时,则不宜用GB/T1278-1994
《化学试剂 氟化氢铵》所讲述的甲醛测铵盐的方法来测定,而应该按GB28655-2012
《工业氟化氢铵》中的直接中和滴定法滴定(预先用饱和硝酸钾液来沉淀掩蔽氟硅酸根的干扰)。4.2.1
原理:用硝酸钾液来沉淀掩蔽氟硅酸根的干扰,以溴百里酚蓝-中性红(pH
≈7.2
)为指示剂,用氢氧化钠标液直接进行酸碱滴定。相关的化学方程式:SiF62++ 2K+ = K2SiF6↓(沉淀掩蔽氟硅酸根的干扰)
K2SiF6+3H2O(热水)=4HF+H2SiO3+2KF(为什么要用碎冰来降温)
NH4HF2 = HF + NH4F
HF+ NaOH= NaF+ H
2O
故这个滴定分析存在着这样的化学计量关系:NaOH
:NH
4HF
2 = 1
:1
可以推导出GB28655
公式中的计算系数:0.05704g/mmoL
。4.2.2
指示剂的选择:同样是酸碱滴定,化学试剂氟化氢铵中氟化氢铵含量的测定要用酚酞(终点pH9.0
),
而工业氟化氢铵中氟化氢铵含量的测定滴定的终点却要在7.2
左右(用溴百里酚蓝-中性红(pH7.2
))?
原因:(1
)如果以酚酞为指示剂,滴定的终点pH9.0
,滴定液中沉淀掩蔽氟硅酸铵的干扰而生成的氟硅酸钾(另外滴定时温度也要控制小于35
度)将发生分解,此时会多消耗部分氢氧化钠用于沉淀的分解,测定结果将偏高。 分解反应:K
2SiF
6↓ +4NaOH=SiO
2+2KF+4NaF+2H
2O
(2
)掩蔽了氟硅酸根后,即可用氢氧化钠标液直接滴定HF
了,NH
4HF
2的组成相当于NH
4F+ HF
,选择合适的指示剂,可以保证只滴定HF
至NaF
,而不会将铵根转化成氨,所以GB28655
中使用了溴百里酚蓝-中性红(pH7.2
),这个滴定同样也不能使用酚酞,因为酚酞指示的终点PH
≈9.0
,此时将有35.8%
的铵根转化为氨了(见下式的计算),故测定所得的氟化氢铵含量就严重偏高了。用氨分布分数来计算pH7.2和pH9.0时铵根转化为氨的百分率:![]()
![]()
发生下列的反应:SiF62-+4NaOH=SiO2+2F-+4NaF+2H2O
故1moL
的氟硅酸铵多消耗6moL
的氢氧化钠,
而这部分的氢氧化钠将被计入氟化氢铵含量中。故有1
份(克数)的氟硅酸铵即相当于6*28.52/178.16=0.96
份(克数)的氟化氢铵(虚高);要将这部分忽略不计的话,
则须≤0.5%/0.96=0.5%
因而有的企业工业产品氟化氢铵的含量用甲醛法来测定的话,
如果该产品的氟硅酸铵含量为2.0%
的话,
那么由它所贡献的氟化氢铵的含量则为:2.0 %*0.96 =1.92%
,即实测值要比真实值高了1.92%
。故只有当工业产品氟化氢铵中的氟硅酸铵含量低于0.5%
时,其氟化氢铵的含量才可以使用GB/T1278-1994
《化学试剂 氟化氢铵》中写到的甲醛法。结论:本文从滴定分析原理、指示剂的选择详细讲述了化学试剂与工业产品氟化氢铵含量的分析方法差别,其差别的原因主要在于工业产品氟化氢铵中所含有的氟硅酸,并指出当工业产品氟化氢铵中的氟硅酸铵含量低于0.5%
时,两个滴定方法才可以互相通用的。参考文献[1] GB/T1278-1994《化学试剂氟化氢铵》[2] GB28655-2012《工业氟化氢铵》