维权声明:本文为Ins_78d530f3原创作品,本作者与仪器信息网是该作品合法使用者,该作品暂不对外授权转载。其他任何网站、组织、单位或个人等将该作品在本站以外的任何媒体任何形式出现均属侵权违法行为,我们将追究法律责任。
可以稀释,但是只能有条件稀释,不能不考虑溶液本身性质,任意去稀释。这是因为Zeta电位本身的属性决定的,Zeta电位本身考虑的是溶液的性质,所以体系的环境非常重要。
Zeta电位是溶液中带电颗粒吸附了溶液中的电荷稳定之后,滑移层的电势。
如果溶液性质改变了,比如H离子或者OH离子,或者其它的阴离子、阳离子的浓度发生了变化,或者盐浓度改变了,均会影响Zeta电位的变化。
为了考察溶液本身酸碱稳定性,可以做Zeta电位随PH变化的曲线,也叫PH滴定。
当然可以滴定的不仅仅是PH值,也可以做其它的添加剂或者盐浓度变化的滴定实验,以便观察Zeta电位随之的变化规律。
如体系中加碱示意图:
溶液中加碱,溶液中游离的OH根离子变多,颗粒携带的负电荷会增多,因此Zeta电位会发生变化,甚至发生反转。
![]()
所以,测试电位不能任意稀释,溶液的PH、离子浓度或者盐浓度变化,均会影响测定结果。
解决办法
:A:可以选择原有配方溶液进行稀释;
B:如果无法得到原配方体系,可以
尝试离心或者沉降的方法,取清液进行稀释,该溶液最接近原液的性质,可以当做稀释液使用,基本不会改变原来的Zeta电位值。
例如,有些溶液体系很浓,直接原液加入浓度太高,光难以穿过样品。我们可以采用离心的方法获取清液,得到的清液再稀释原液,得到合适的浓度,再进行电位测试。
![]()
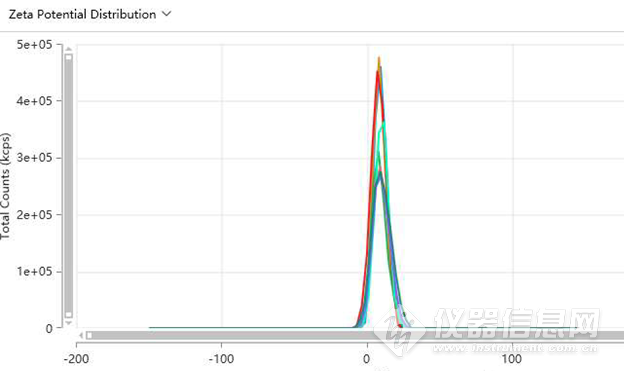
不同浓度的清液稀释样品,电位值变化不大。
![]()