对于制剂,有关物资可能是存在在活性物质中的杂质、降解物、赋形剂与活性物质的相互作用产物、额外的成分,如从赋形剂或制造过程中引进的残留溶媒;以及从容器和密闭包装或从制备过程中引进的可滤过和可提取的杂质。
药物加速试验的数据要上报,根据申报的药品和“Guideline for Submitting Samples and Analytical Data for Methods validation”的要求,使用酸、碱水解、温度、光分解、氧化等方法进行加速试验。样品、包括杂质、防腐剂以及空白样品等的加速或不加速的样品的有代表性的色谱图要上报。与杂质试验方法一起,色谱图应表明存在的杂质的检出限 / 定量限要求。色谱图应该是清楚的、有标识的、有时间或时间刻度并且衰减应标明。
注意点
1.主峰可以扩展,如通过增加浓度、改变衰减使可以见到大小合适的额外峰以评价反映稳定性的能力。见.B部分检出限和定量限的建议。
2.基线应在刻度上面 ,因离开刻度的基线(见到的是一条平直的线)可能掩盖小峰。
峰的纯度通过二极管阵列检测器测定,然而目标化合物中存在的低浓度的额外化合物可能不干扰或不影响分析物的UV光谱。
图3和图4说明用二极管阵列检测器的UV光谱图和色谱图。(a)为三维色谱图,(b)为普通色谱图。分析物在4.7分钟流出,应该注意UV光谱图的质量对低浓度化合物是差的。
当用加速试验的样品时,应选择合适的检测器和积分仪,如为能检测0.1%低浓度的降解物,母体峰的检出限至少是0.1%,或面积计数是合理的。
建议
加速和未加速的样品的有代表性的色谱图应上报。包括杂质试验方法、防腐剂等,连同有关的空白样品也一起上报。有代表性的色谱图要以加入已知的额外化合物来标明其选择性。
J. 系统适应性规格和试验
HPLC收集的准确度和精密度数据开始于性能良好的色谱系统。系统适应性
规定和试验则是帮助达到这一目的的参数。本节解释图5指出的术语,并提供
建议和说明。
图中Wx为在5%(0.05)或10%(0.10)峰高处测得的峰宽
f 为在W处峰最大值至峰前沿的距离
t0为死体积或不保留成分的洗脱时间
tR为分析对象的保留时间
tW为直线外推基线处的峰宽
1. 容量因子(k'')
k''=(tR-t0)/t0
容量因子是目标峰对死体积,即不保留成分的洗脱时间的比值。
建议
目标峰应该与其他峰和死体积良好地分离。一般k''>2.
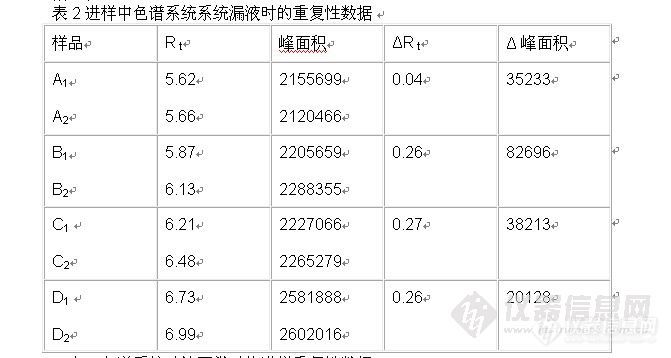
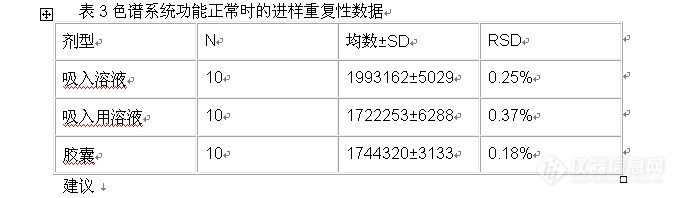
2. 精密度/进样重复性(RSD)
以RSD表示的进样精密度表明了HPLC仪器的性能,包括在样品分析时泵、色谱柱和环境的状况。应注意样品制备和制造的变异未予考虑。
建议
RSD≤1% (n≥5)
3. 相对保留时间(α)
α=k''1/k''2
相对保留时间为两个峰相对位置的比值,这不是象分离度(RS)的规定,不是基本参数。
4. 分离度(RS)
RS=(tR2-tR1)/(1/2)(tW1+tW2)
RS表示两个峰被分离好的程度。对于可信赖的定量分析,良好分离的峰对定量是必要的。
如果考虑可能的干扰峰,分离度是非常有用的参数。应选择与分析对象最接近的可能的洗脱峰。RS最小受两种被测量成分比例的影响。峰的分离度RS如图6所示。
分析对象和最接近的可能干扰峰(杂质,附加剂,分解产物,内标等)的RS >2 是合适的。
5. 拖尾因子(T)
T=Wx/2f
随着峰拖尾因子的增加定量准确性降低,因为要决定何时、在哪里峰结束,这造成积分峰面积的困难。为分析对象峰面积的最佳计算,积分变量是分析者预设的。
图7和图8表明拖尾因子对定量的影响。如果积分仪不能准确决定何时上升或下降,
那么准确性就要降低。
建议
T≤2
6. 理论塔板数(N)
N=16(tR / tW)2 = L/H
理论塔板数是对柱效的测量,它表示在单位色谱运行时间内可以有多少个峰。
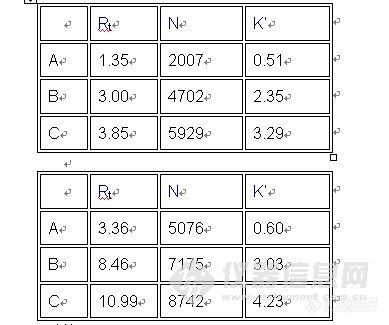
在一套固定的色谱操作条件下,每个峰N 基本恒定。H或者HETP为每个塔板相当的高度,测定柱单位高度(L)的柱效。能够影响N或者H的参数包括峰位置、柱内填料颗粒的大小、流动相的流速、柱温、流动相黏度和分析物的分子量。图9表明在两种不同色谱条件下得到的A,B和C三个化合物的色谱图。B的RtS分别为3和8.5分钟。B峰的测定说明尽管出现的峰相似,但理论塔板数是不同的。
![]()
建议
理论塔板数取决于保留时间,但一般应>2000。
一般建议
系统适应性试验对于保证色谱系统的高性能是重要的。试验要求的数量取决于试验方法的目的。对于溶出度,释放度这类试验方法k'',T,和RSD是最低推荐的系统适应性试验。对于验收、出厂、稳定性试验、或杂质和降解物的测定,用外标法或内标法;k''、T、Rs和RSD被推荐为最低系统适应性参数。实际上验证每一种方法都应当适宜数量系统适应性试验,以规定必要的系统特性。在申请者和评审者慎重时,可选择附加试验。
K. 要点
试验方法中应该注意的某些基本点
1.样品和对照品都应该溶解于流动相中,如果不可能,避免使用比流动相浓度
高得太多的有机溶剂。
2.样品和标准品浓度如果不同,应该接近。
3.样品在分析过程中应该用标准品同时测定
4.进样前样品过滤有时碰到。过滤将除去能填塞柱子的颗粒。分析对象被吸附也能发生,这对低浓度杂质尤其重要。申请者这方面的验证数据要上报。
V. 建议和结论
药物及其制剂的HPLC方法
方法不应该只验证一次,而应该由开发者或者使用者验证和设计以保证方法自始至终的持久稳定性或一致性。
药物制剂制造过程,实验室样品的制备操作和仪器性能变异都影响分析得到数据的准确性。应有适当的验证和严格的色谱性能(系统适应性规定),才能得到更可靠的数据。除药品制造过程以外的变异都应最小化。只有经过良好可信验证过的方法,用于出厂,稳定性和药物代谢动力学的数据才是有价值的。
VI. 致谢
感谢Hoiberg, poochikian, Blumenstein, Look和Tilgyesi博士(HFD-150)
Layoff博士(HFH300)
Zirmmerman和Piechocki博士(HFD-110)
以及分析方法技术委员会的Sheinin博士,Shostak先生,Cunningham女士,
Jongedyk女士,Leutzinger先生,Seggel博士,Sharkey女士和Smela先生
的宝贵建议。
VII. 参考文献
1.Guideline for Submitting Samples and Analytical Data for Methods
Validation ,February 1987.
2.United States Pharmacopeia , ,1990(1225).
3.Text on Validation of Analytical Procedures ,International Conference on
Harmonization ,September 1993.

 色谱方法验证审评指南.doc
色谱方法验证审评指南.doc