使用声力研究蛋白去折叠
单分子力谱(SMFS)技术是研究蛋白结构与蛋白去折叠中的生物力学性质的有力工具。SMFS能够为研究和药物开发提供有价值的信息。SMFS有助于揭示人类疾病病理的分子机制,而机制往往被认为与错误折叠的蛋白的形成和积聚有关,如阿茲海默症和帕金森氏症。
然而现有的SMFS仪器缺少同时并行研究多个蛋白去折叠的功能,使得研究过程耗时很长。使用声波来对数以百计的生物分子施力并操控是非常理想的高通量研究方法。此案例中,声力谱学(AFS)是最新的用于研究蛋白去折叠的单分子操控方法。
![]()
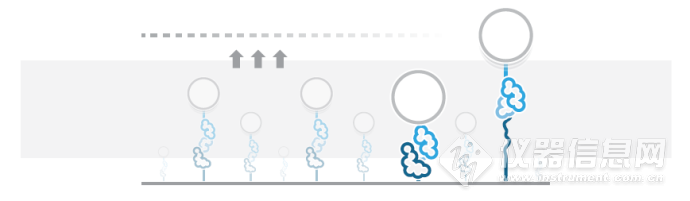
1 AFS检测蛋白去折叠的图解。蛋白一端栓住玻璃表面,另一端拴住聚苯乙烯微球。
![]()
2 对视野范围内被蛋白分子拴在玻璃表面的4.5 μm聚苯乙烯微球同时成像。物镜放大倍数为20x。
AFS设备使用压电元件共振激发平面声阱穿过微流控芯片。共振波对与周围介质密度不同的微球施力,每个生物分子被单独地由微球拉伸(图1)。仪器可以实时并行操控视野范围内数以百计的微球,获得大量的数据以研究每个生物分子的随机与异质行为(图2)。在Yan Jie(NUS)的实验室的这项试点研究中,我们首次展示了AFS如何对蛋白施力并操控。实验对踝蛋白施力引发(去)折叠同时以高精确度记录蛋白的拉伸。踝蛋白属于机械敏感性大分子,在调控蛋白粘附于胞外基质中起作用。踝蛋白是细胞代谢过程和信号通路中的关键,并能够在力的作用下改变构象,在单分子生物物理学中备受关注。
![]()
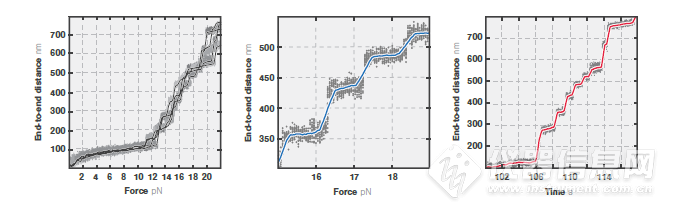
3 使用AFS得到的单个踝蛋白分子的去折叠曲线,力变化速率为1 pN/s。轨迹在500 Hz下获得(彩色点),并平衡至50 Hz(黑色线)。
3a 单个踝蛋白多次拉伸的力-距离曲线。3b 单个拉伸循环的力-距离曲线。3c 图3b中分子的时间-距离曲线。
在这项研究中,连接了DNA的踝蛋白拴在聚苯乙烯微球和玻璃表面。启动声波后形成平面声阱,连接了踝蛋白的微球受到朝向声阱的力。实验中通过调节声波的振幅来改变力的大小。逐渐增加力的大小使得蛋白的结构域按顺序去折叠。实验循环进行拉伸与收缩的过程(力变化速率为1 pN/s)并同时以nm级的分辨率检测每个蛋白的拉伸长度(图3)。通过力-距离曲线(图3a)可以观察到单个踝蛋白的去折叠循环。将单个蛋白的去折叠轨迹叠加即可检测到单个结构域去折叠的发生,研究人员可以得到蛋白结构和蛋白去折叠自由能图谱信息。
AFS仪器产生的超声并不会损害生物分子的结构完整性,因此蛋白可以连续去折叠和再折叠长达数小时,并能够得到单个蛋白多次去折叠和再折叠的曲线。相比于其他SMFS方法经过多次拉伸和收缩之后对蛋白造成光学损伤或力学损伤使得实验被迫终止,AFS能够获得更多的信息。
图3b: 单个力-距离曲线中截取一小段,表示一个拉伸过程。将力从15 pN增加至19 pN,可以观察到4个去折叠过程,与蛋白的4个结构域相符合,拉伸长度为30 nm至100 nm。AFS的高分辨率检测功能可以很清晰地区分去折叠过程。AFS在x,y方向精度为2 nm,在z方向精度为4 nm(频率为25 Hz),可以大幅提高(去)折叠研究的精密程度。图3c: 图3b中分子的18秒范围内的时间-距离曲线。AFS可以检测短至毫秒级至长达10小时以上的事件,用于研究蛋白的热力学和动力学。
通过检测踝蛋白的去折叠步骤并记录连续的高分辨率的去折叠轨迹,可以得出AFS如何用于研究蛋白去折叠。研究蛋白(去)折叠的详细机制能够在生物物理和生物医药领域产生突破性发现。
今后的蛋白折叠以及蛋白相互作用的研究中,AFS的多分子并行操控功能将发挥重要作用,用户可以同时并行检测大量的蛋白分子。用户可以获得大量的实验数据,在不影响分辨率的同时对蛋白的机械性质数据作出分析。