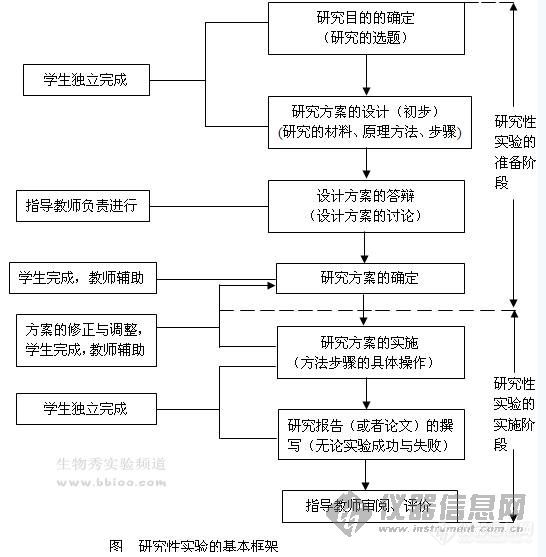
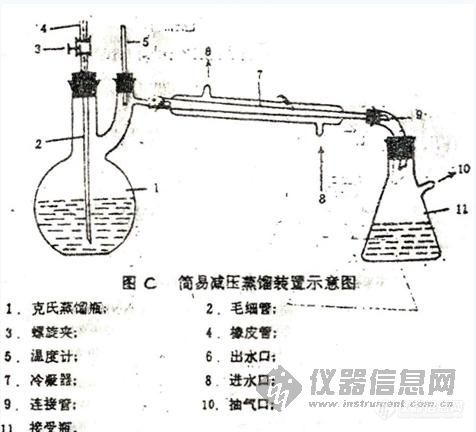
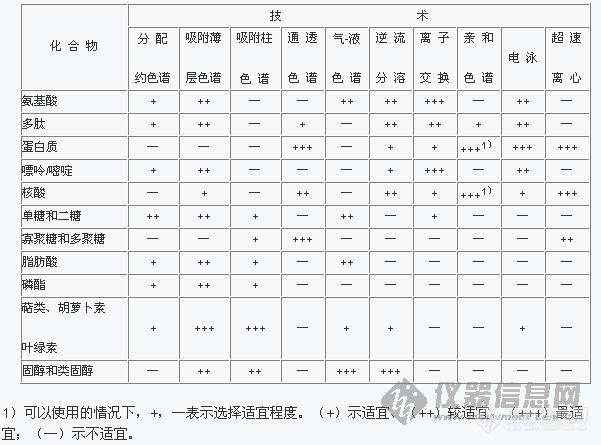
2)物理法主要通过各种物理因素使组织细胞破碎的方法。在生化制备中常用的有:
①反复冻融法:先将样品深冷至—15℃至—20℃使之冻固,再缓慢地融化,反复多次可将大部分细胞破碎,此法多用于动物性材料。
②急热骤冷法:将样品材料投入沸水,维持85—90℃数分钟后,置冰浴中急速冷却,使细胞壁结构受到破坏。此法可用于细菌及病毒材料,但制备对热敏感的物质时慎用。
③超声波处理:此法多用于微生物材料,频率一般选在10KC至200KC,功率200—500瓦范围,对于不同细菌,应视具体情况而定。处理时间有数分钟至数十分钟不等。处理效果和样品浓度及使用功率有关。在处理过程中如溶液温度升高时,注意冷却。
(3)化学及生物化学法 主要有自溶法,酶解法和表面活性剂处理法等。
①自溶法:自溶法是在一定的pH和适当的温度下,利用组织细胞内自身的酶系统将细胞破碎的方法。自溶法所需时间较长,常添加少量防腐剂如甲苯、氯仿等防止细菌的污染。
②酶解法:利用各种水解酶如溶菌酶,纤维素酶、“蜗牛”酶、半纤维素酶、壳糖酶、脂酶等专一性地将细胞壁分解,使细胞内含物释放出来。适用于制备大分子核酸材料的破壁。有些细菌对溶菌酶不敏感,加入少量巯基试剂或8mol•L-1脲素处理后,使转为对溶菌酶敏感而融溶。
③表面活性剂处理:如十二烷基硫酸钠、氯化十二烷基吡啶、去氧胆酸钠等均对细胞膜有一定破坏作用。
此外,使用真空干燥及冷丙酮处理制成“丙酮粉”均可以改变细胞的透性,不同程度地破坏细胞膜结构,以利于提取。
有时为了防止其他细胞组份中的物质对制备物干扰或污染,或由于对细胞组分上某一物质进行特殊研究的需要,常将各种细胞器先行分离,然后在某一细胞器中提纯某一物质。细胞组份的分离,一般使用差速离心法,即将破碎后细胞在适当介质中进行离心。常用的介质有生理盐水,蔗糖或葡萄糖-聚乙二醇等高分子溶液。各种细胞组份按照质量、大小不同,经过不同速度的离心后,便沉降于离心管不同部位,经过多次分步离心分离,即可获得所需要组份。
组织细胞破碎过程中,大量胞内酶及细胞内含物被释放出来,须立即选择适当条件进行提取分离,避免因长久放置造成制备物的分解破坏。
提取是分离纯化的第一步,它将制备物从复杂的生物体系中转移到特定的人工
液相体系中(通常是水、缓冲液,稀盐溶液或有机溶剂)。提取所用的溶剂的选择标准首先对被制备物具有最大溶解度,并在提取中应尽可能减少一些不必要的成份。为了更好地达到以上两个目的,常用的手段是调整溶剂的pH值、离子强度、溶剂成份配比和温度范围等。
(四)抽提液的浓缩
一般抽提液的体积都比较大,应先进行浓缩处理。常用的浓缩方法有下面几种:
1.沉淀法
在抽提液中加入适量的中性盐[如(NH4)2SO4]或有机溶剂,使有效成分变为沉淀。经离心或过滤收集的沉淀物,加少量缓冲液溶解后,再经离心除去不溶物,获得的上清液通过透析或凝胶过滤脱盐,即可供纯化使用。
2.吸附法(吸水法)
将干葡聚糖凝胶G25(或吸水棒)加入抽提液中,两者比例为1∶5。由于凝胶吸水之故,抽提液的体积可缩小三倍左右,回收蛋白质量约80%。当凝胶(或吸水棒)对有效成分吸附力强或吸水后对有效成分的性质有影响时,此法不宜采用。
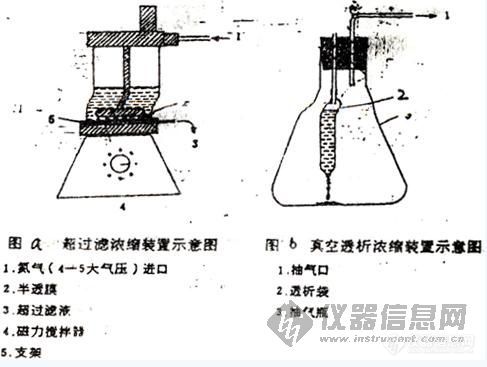
3.超过滤法
把抽提液装入超过滤装置(见图a),在空气或氮气(5个大气压)压力下,使小分子物质(包括水分)通过半透膜(如硝酸纤维素膜),可使50毫升样品在12小时内深缩到5毫升。
![]()