
获得0积分,您同时完成了每日任务,有额外的积分奖励,请前往APP领取
立即前往
原文由 rainyunzhang 发表:
请问哪位同仁用GBZ/T160.33-2004的方法测定过空气中的硫化氢(硝酸银比色法)?
我不太理解标准溶液为什么使用硫代硫酸钠(硫代硫酸钠中的硫如何转化为负二价的硫离子,然后与硝酸银生成沉淀?),还有加淀粉的作用是什么?吸收液为什么用亚砷酸钠和碳酸铵的混合溶液(亚砷酸钠的作用是什么)?
用目视比色法很难观察,请问各位是在多少波长下测定?



原文由 emily09 发表:
我今天也做硫化氢的测定,就是不知道用哪个波长测,然后做了个光谱分析,得到它的最大吸收在235nm,用这个波长测它的吸收,合适吗?
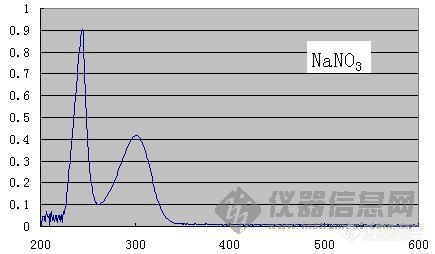
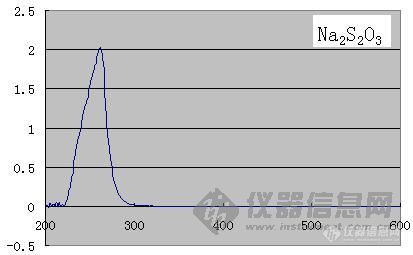
 GBZ_T 160.33-2004(H2S)
GBZ_T 160.33-2004(H2S)