进样瓶和样品存储瓶是实验过程,特别是色谱实验过程不可或缺的最基础工具。虽然与实验室使用的众多精密的分析仪器相比,自动进样瓶看似无关紧要的,但进样瓶或盖、垫的错误使用却会给实验带来重大影响,导致实验效率和重复性的降低。错误使用样品瓶/盖/隔垫可能导致的潜在问题包括:挥发导致的分析物损失;溶剂与隔垫作用产生的色谱杂峰;自动进样器的机械损坏;样品降解;进样重复性差等等。
新买的样品瓶,大多都是硅烷化去活的瓶子。国外的实验室,一般进样瓶是一次性的。但考虑到国情,咱们国内实验室使用的样品瓶,几乎都是反复使用的,水、洗涤剂、有机溶剂清洗,或者象我们实验室一样,400-500度的高温灼烧。有机物残留是没有了,硅烷化涂层也没有了,于是,玻璃表面的强极性的硅羟基暴露出来,会对一些物质产生吸附,特别是在含量很低的时候,造成很大的误差。
拿一组伏马菌毒素的数据来说明问题。
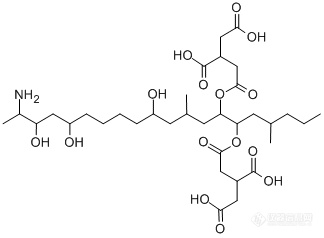
伏马菌素 (Fumonisin FB) 是一种霉菌毒素,是由串珠镰刀菌 (Fusarium moniliforme Sheld)产生的水溶性代谢产物,是一类由不同的多氢醇和丙三羧酸组成的结构类似的双酯化合物。常见的有FB1、FB2、FB3。
伏马菌毒素B1的分子量为721.83,伏马菌毒素B2和B3的分子量均为705.83;伏马菌毒素B1的同位素内标的分子量为755.83;伏马菌毒素B2和B3的同位素内标的分子量为739.83。
上一个伏马毒素B1的结构式
![]()
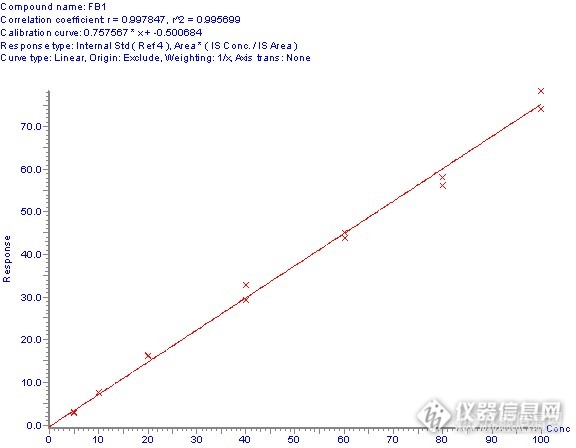
通常我们使用的就是反复烧过的瓶子,配了一条标准曲线,伏马毒素B1的浓度分别为5、10、20、40、60、80、100ng/ml,同位素内标的量为10ng/ml。于是神奇的事情出现了。
看看标准曲线还好,
![]()
再看看同位素内标的峰面积分布,惨不忍睹,严重失散。
![]()
再看数据,发现浓度越低的点,同位素内标的峰面积越小, 浓度从低到,同位素的峰面积也逐渐增大。
![]()
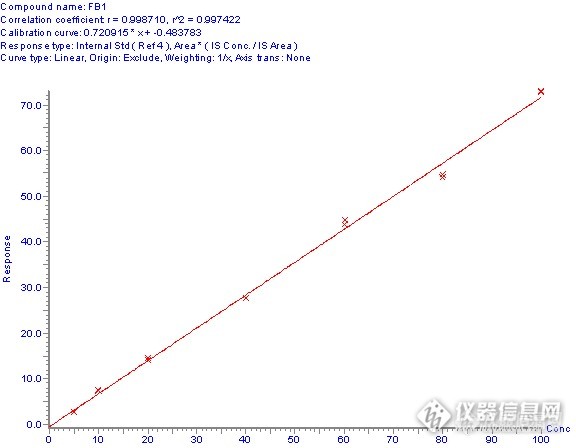
果断更换新的进样瓶,重新配制一条标准曲线,线性相差不多。
![]()
但同位素内标峰面积的分布很集中,
![]()
再看数据,不同浓度的各点,同位素内标的峰面积相差不多。
![]()
真是伤不起呀,如果不是利用同位素内标法定量,这条标准曲线不知道要偏到哪里去了。啥时候咱们也象老外一样一次性使用呀。
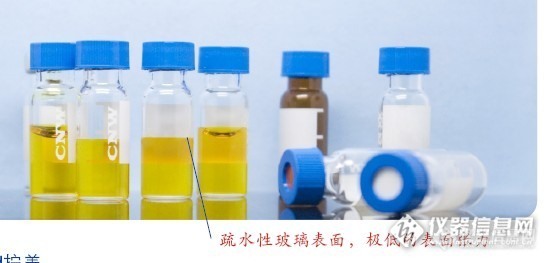
现在能买到的进样瓶,有去活和不去活,很容易分辨的,装上溶液,看液面,去活过的瓶子的液面会比较平的,没去活的瓶子的液面是弯弯的月牙形。
![]()
想起安谱以前的促销
![]()
![]()