3月2日,清华大学生命科学院
施一公教授领导的研究组与
王佳伟副教授合作在《自然》在线发表论文,报道原核细胞蛋白酶体调节亚基MecA-ClpC异六聚体结构与功能的研究。
ATP依赖的可调控蛋白质水解广泛存在于大多数生命体中,对于及时清除机体内的垃圾蛋白以及调节蛋白具有十分重要的作用。原核生物中负责这一功能的蛋白酶体由调节亚基-Clp/Hsp100家族成员同催化亚基ClpP两部分组成。研究发现,Clp/Hsp100家族蛋白都是以六聚体形式执行功能。ClpC是Clp/Hsp100家族的重要成员,含有两个AAA+(ATPasesassociatedwithdiversecellularactivities)结构域(核酸结合结构域),与该家族其它成员不同的是,ClpC的六聚体形成及其进一步的激活需要接头蛋白MecA的参与。利用ATP水解的能量,激活后的六聚体MecA-ClpC分子能够去折叠特异性蛋白质底物,并将生成的去折叠多肽链转运到ClpP中降解。但是,MecA如何介导ClpC形成六聚体并激活ClpC的分子机制一直都没有明确的解释。
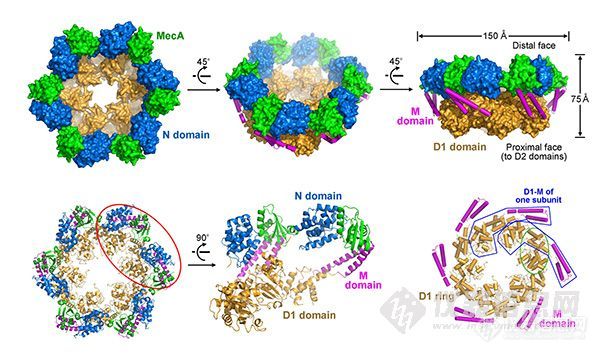
自2007年6月起,施一公教授领导的该课题组一直致力于对原核细胞内蛋白酶体调控机理的研究。经过3年多的艰辛努力,该课题组首次解析了枯草芽孢杆菌内蛋白酶体调节亚基MecA-ClpC复合物的三个相关晶体结构,并结合大量的生化实验数据,揭示了六聚体MecA-ClpC复合物的组装方式,阐明了MecA介导ClpC激活的分子机理,并提供了MecA-ClpC执行功能的结构基础。这些发现对揭密其它Clp/Hsp100分子机器的组装方式也有很好的借鉴作用,并且为研究真核生物内更为复杂的泛素-蛋白酶体系统提供了方法论和实验基础。(来源:清华大学生命科学院)
![]()