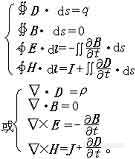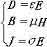热力学第一定律
thermodynamics,first law of
普遍的能量转化和守恒定律在一切涉及热现象的宏观过程中的具体表现。热力学的基本定律之一。
表征热力学系统能量的是内能。通过作功和传热,系统与外界交换能量,使内能有所变化。根据普遍的能量守恒定律,系统由初态Ⅰ经过任意过程到达终态Ⅱ后,内能的增量ΔU应等于在此过程中外界对系统传递的热量 Q 和系统对外界作功A之差,即
UⅡ-UⅠ=ΔU=Q-A或Q=ΔU+A这就是热力学第一定律的表达式。如果除作功、传热外,还有因物质从外界进入系统而带入的能量Z,则应为ΔU =Q-A+Z。当然,上述ΔU、A、Q、Z 均可正可负 。对于无限小过程,热力学第一定律的微分表达式为
dQ=dU+dA因U是态函数,dU 是全微分;Q、A是过程量,dQ 和 dA只表示微小量并非全微分,用符号d以示区别。又因ΔU或 dU 只涉及初、终态,只要求系统初、终态是平衡态,与中间状态是否平衡态无关。
热力学第一定律的另一种表述是:第一类永动机是不可能造成的。这是许多人幻想制造的能不断地作功而无需任何燃料和动力的机器,是能够无中生有、源源不断提供能量的机器。显然,第一类永动机违背能量守恒定律。
热力学第二定律
thermodynamics,second law of
关于一切涉及热现象的实际宏观过程方向的热力学定律。它指出,一切涉及热现象的实际宏观过程都是不可逆过程。
机械运动、电磁运动中的各种不涉及热现象的过程都是可逆的,可以正向进行,也可以逆向进行,逆过程的每一步都与正过程相同,只是次序相反。但是,功变热量、热传导、自由膨胀等涉及热现象的过程却都不能自动地逆向进行,使系统和外界完全复原。热机把热变为功,热力学第一定律断言其效率不可能大于1,但能否接近或达到100%呢?换言之,物体的机械能可以通过摩擦、阻尼、内耗等方式自发地全部转化为系统的内能;反之,系统的内能能否自发地转化为机械能而不产生其他影响呢?卡诺定理指出,这是不可能的 ,因为存在着某种理论上的限制。由此可见,尽管热量和功都是传递的能量,都是过程量,可按热功当量换算;但也有重要的区别,作功是通过系统整体的宏观位移实现的,传热则是通过组成系统的大量分子的无规则热运动和相互之间的作用实现的。热功转换是系统内分子无规则热运动能量与系统有规则整体运动能量之间的转换。这种转换不仅在总量上要守恒以满足热力学第一定律,而且还必须在转换的方向和限度上受到限制。这正是热运动区别于其他运动形式的特殊本质。热力学第二定律就是这一特征的概括。
热力学第二定律有多种表述方式,常用的是以下两种 。①开尔文表述:不可能从单一热源吸取热量,使之完全变为有用的功而不产生其他影响。或第二类永动机是不可能造成的。第二类永动机是能从单一热源吸取热量并使之完全变为有用的功而不产生其他影响的机器。虽然,它并不违反第一定律。②克劳修斯表述:不可能把热量从低温物体传到高温物体而不产生其他影响。这两种表述分别揭示了热功转换过程和热传导过程的不可逆性。可以证明两种表述完全等价 。这表明,各种不可逆过程具有深刻的内在联系。因此,可以选用任何一种特殊的不可逆过程来表述普遍的规律。无论采用何种表述,热力学第二定律的实质是指明,在一切涉及热现象的实际宏观过程中,能量转换或传递的方向、条件和限度。
态函数熵为热力学第二定律提供了定量表述,熵的微观含义揭示了热力学第二定律的微观本质和统计意义。
热力学第三定律
thermodynamics,third law of
通常表述为绝对零度时,所有纯物质的完美晶体的熵值为零。
1906年W.H.能斯脱在实验的基础上提出:当温度趋近于绝对零度(0K)时,凝聚物系等温过程的熵变ΔS也趋近于零:
![]()
此即能斯脱热定理 ,也可看 作是第三定律 最 早的表述形式。它意味着,当温度趋近于0K时,所有凝聚物系的熵值趋近于一个相同的极限值。1912年M.普朗克在能斯脱热定理的基础上,进一步假设当温度趋近于0K时,所有纯液体和纯固体的熵值为零。然而后来的实验事实和统计热力学对熵的讨论都表明,有些纯态物质(如过冷液体和某些固态化合物)在温度趋近0K时,仍有一个正的熵值。因此G.N.路易斯和M.兰德尔将普朗克的假设修正为:在0K时,所有纯物质的完美晶体的熵值为零。所谓完美晶体是指系统内部已经处于热力学平衡的晶体,因此热力学第三定律又可表述为:对于热力学系统中每一个达成内部平衡的方面来说,它对系统的熵的贡献一定会随热力学温度同趋于零。
根据热力学第三定律,欲求纯物质在某指定状态下的熵值,只要利用热容、相变焓等热力学数据,计算出此物质从绝对零度的完美晶体至指定状态下的熵变 ΔS ,即为该状态下此物质的熵值,称为规定熵或第三定律熵。在温度为 T 时,处于标准状态的单位物质的量的物质 B 的规定熵称为在此温度下物质B的标准摩尔熵,记作(B,T)。常见物质在 298K的值可自手册上查到。
1940 年R.H.否勒和 E.A.古根海姆还提出热力学第三定律的另一种表述形式:任何系统都不能通过有限的步骤使自身温度降低到0K,称为0K不能达到原理。此原理和前面所述及的热力学第三定律的几种表述是相互有联系的。但在化学热力学中,多采用前面的表述形式。
老西忘了重要的一条,我给你补上:
热力学第零定律:如果两个热力学系统中的每一个都与第三个热力学系统处于热平衡,那么它们也必定处于热平衡。
热力学第零定律于1930年由福勒(R.H.Fowler)正式提出,比热力学第一定律和热力学第二定律晚了80馀年。虽然这么晚才建立热力学第零定律,但实际上之前人们已经开始应用它了。因为它是後面几个定律的基础,在逻辑上应该排在最前面,所以叫做热力学第零定律。

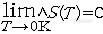
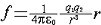
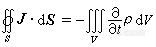
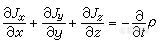

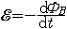
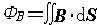
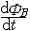 闭合回路中感应电流的方向 。在规定回路绕行方向后,按右手螺旋定则确定曲面的法线方向n。若B与n夹角为锐角 ,ΦB取正值;为钝角 ,ΦB取负值。然后,根据磁通量的实际变化情况,确定的正负 ,再由定律可知的正负 。若为正值 ,表示构成感应电动势的非静电力的方向与回路绕行方向一致 ;为负值,相反。由非静电力的方向即可确定回路中感应电流的方向。
闭合回路中感应电流的方向 。在规定回路绕行方向后,按右手螺旋定则确定曲面的法线方向n。若B与n夹角为锐角 ,ΦB取正值;为钝角 ,ΦB取负值。然后,根据磁通量的实际变化情况,确定的正负 ,再由定律可知的正负 。若为正值 ,表示构成感应电动势的非静电力的方向与回路绕行方向一致 ;为负值,相反。由非静电力的方向即可确定回路中感应电流的方向。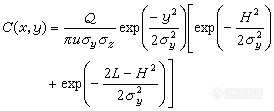
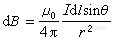
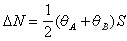

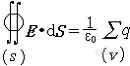
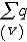 是V内自 由电荷 的代数和,在有电介质时,
是V内自 由电荷 的代数和,在有电介质时,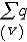 V内自由电荷和极化电荷的代数和 。
V内自由电荷和极化电荷的代数和 。