维权声明:本文为qindong413原创作品,本作者与仪器信息网是该作品合法使用者,该作品暂不对外授权转载。其他任何网站、组织、单位或个人等将该作品在本站以外的任何媒体任何形式出现均属侵权违法行为,我们将追究法律责任。
NIRS用于桂枝中桂皮醛、水分、浸出物含量快速检测方法研究
研究生:范剑
导师:臧恒昌教授
摘要目的:干姜和桂枝为传统常用药对。现代药学研究表明,桂枝、干姜均含有大量挥发油且为两药主要药效成分。随着2016年《中药配方颗粒管理办法(征求意见稿)》发布,未来中药配方颗粒限制将逐步放开。相对于单味药材提取的配方颗粒,经典药方或药对形式的配方颗粒,因其更加贴近中医用药理论,将来会受到越来越多的重视。进行干姜和桂枝混合蒸馏提取过程的研究,也可为经典药对配方颗粒的开发提供一定的技术支持。
方法:采用 Antaris II 傅立叶变换
近红外光谱仪漫反射模块采集85批桂枝样品
近红外光谱,以甲苯法、超高效
液相色谱法和浸出物测定法,分别测定样品中水分、桂皮醛和浸出物含量,作为参考值,结合偏最小二乘算法分别建立水分、桂皮醛和浸出物含量的快速定量模型。
关键词:桂枝;
近红外光谱;过程分析
The research on the mixeddistillation extraction of Zingiberis Rhizoma and Cinnamomi Ramulus by NIRS
Grauate student: Jian Fan
Supervisor:Hengchang Zang
Abstract Objective:Zingiberis Rhizoma and CinnamomiRamulus are couplet medicinesa in the Traditional Chinese Medicine (TCM). TheZingiberis Rhizoma contains chemical constituents of volatile oil, gingeroletc. It is a common TCM used in medicine and food. Its ether extract and waterextract have obvious analgesic effect. The cassia twig mainly contains cinnamicacid and cinnamaldehyde, it has obvious antipyretic, sedative, antiasthmatic,anti allergic and other effects. TCM on Guizhi - ginger in the compound oftraditional Chinese medicine compatibility is widely used, such as ZhangZhongjing, there are Guizhi drug compatibility in Huang Liantang, smallQinglong Decoction, Chaihuguizhi dried ginger in the “Treatise on FebrileDiseases”. Cassia twig and dried ginger contain a lot of volatile oil, and theyare the main active ingredients of two drugs. Shenzhiling oral solution is onenew kind of traditional chinese drugs , in the production of it,Zingiberis Rhizoma and CinnamomiRamulus as a couplet medicinesa were extracted together; in 2016, theregulation of Chinese Medicine Dispensing Granules(take advicing)wes published. In thefuture, the limitations of Chinese Medicine Dispensing Granules will begradually liberalized, the application amount of Chinese Medicine DispensingGranules will be greatly increased. Chinese Medicine Dispensing Granules madewith a classic prescription of Chinese Medicine or couplet medicinesa. In thefuture, more and more attention will be paid to it. Study of ginger and CinnamomiRamulus mixed distilled extraction process, but also can provide technicalsupport for the development of the classic of medicine formula granules.
Methods: Collect 75 near infraredspectroscopys of samples by near-infrared spectrograph with diffuse reflectancemodule. The reference analyses were performed with toluene methodand, UHPLC andpharmacopoeia method respectively for determination of cinnamaldehyde,moisture, and extraction.
Key words: near-infraredspectroscopy; manufacture process; process analysis techonlogy
1 材料与仪器
1.1 试剂与样品 桂皮醛(纯度 98.9 %,批号 110710-201619)购自中国食品药品检定研究院;乙腈、甲醇均为色谱纯;甲苯为分析纯加水饱和后经蒸馏制得;其它等试剂均为分析纯;超纯水(自制);75批桂枝样品购自零售药店、医院药房及药材批发企业,经泰安市食品药品检验检测中心中药科鉴定为樟科植物肉桂的干燥嫩枝。
1.2 仪器和软件Antaris II傅立叶变换
近红外光谱仪,PLS_Toolbox工具箱;Agilent 1290型超高效
液相色谱仪;Aquity BEH C18 色谱柱;KQ-100DE型医用数控超声波清洗器;电子分析天平; FW80型高速万能粉碎机。
2 方法
2.1样品制备将收集的75批桂枝药材粉碎过40目筛,编号,封口袋密封置防潮柜中常温保存,备用。
2.2 近红外光谱的采集取样品粉末约5g,混合均匀后放入样品杯中,摊平,压紧,以空气为参比,扣除背景,采用积分球漫反射方式采集
近红外光谱图。光谱扫描范围4000~10000 cm
-1,分辨率8 cm
-1,扫描次数32次,每批样品扫描3次,求平均NIR光谱值。
2.3 样品中桂皮醛含量的测定(1)对照品溶液的配制
精密称取桂皮醛对照品105.00 mg于100 mL容量瓶中,加甲醇溶解并稀释至刻度,再精密量取1 mL至100 mL量瓶中加甲醇稀释至刻度。
(2)供试品溶液的制备
取桂枝粉末约0.5 g,精密称定,置具塞锥形瓶中,精密加入甲醇25 mL,称定重量,超声处理30分钟,放冷,再称定重量,用甲醇补足减失的重量,摇匀,滤过,精密量取续滤液1 mL ,置25 mL量瓶中,加甲醇至刻度,摇匀,即得。过0. 2 μm 微孔滤膜,供UHPLC分析用。
(3)色谱条件
WatersAquity BEH C18 色谱柱;流动相水(A)-乙腈(B),梯度洗脱;柱温30 ℃,流速0.3 mL/min,检测波长280 nm,进样体积5 uL。
(4)含量测定
按照(2)项下供试品溶液配制方法配制各样品供试品溶液,在(3)项的色谱条件下进样分析,利用外标法计算桂皮醛的含量。
2.4 样品中水分含量的测定按照2.2.4项下方法,精密称取样品粉末约15 g,测定计算含量。
2.5 样品中浸出物含量的测定 供试品约2 g,精密称定,置100 mL的锥形瓶中,精密加水50mL,密塞,称定重量,静置1小时后,连接回流冷凝管,加热至沸腾,并保持微沸1小时。放冷后,取下锥形瓶,密塞,再称定重量,用水补足减失的重量,摇匀,用干燥滤器滤过,精密量取滤液25 mL,置已干燥至恒重的蒸发皿中,在水浴上蒸干后,于105 ℃干燥3小时,置干燥器中冷却30分钟,迅速精密称定重量。以干燥品计算供试品中水溶性浸出物的含量(%)。
2.6 定量模型的建立利用化学计量学软件对光谱数据进行处理,建立桂枝中桂皮醛、水分、浸出物含量的PLS定量分析模型。首先,用K-S法按照2:1比例对样品进行校正集和验证集划分;通过光谱预处理方法和建模光谱区间的选择优化建模参数,提高模型稳健性和预测能力。采用模型评价参数 RMSEC、RMSEP、
R2c、
R2P、
LVs等参数对模型准确度和预测能力进行评价,并利用配对
t检验对验证集预测结果与测量结果进行显著性检验,进一步评价模型的预测能力。
3 结果与讨论
3.1 桂皮醛含量结果(1)UHPLC分析方法线性考察
UHPLC分析方法线性考察结果:桂皮醛与相邻杂质峰分离度均大于1.5,符合分离度要求,在1.05-21 ug/Ll范围内,标准曲线为y = 166634x + 17.599 ,r
2 =0.9998,标准曲线线性良好。图3-1为桂皮醛测定中,对照品与样品色谱图。
![]()
![]()
A.对照品;B.样品;
图3-1 桂枝中桂皮醛含量测定对照及样品的UHPLC
(2)桂皮醛含量结果
共测定75个样品,其桂皮醛含量范围在0.543 % ~1.83 %。
3.2 水分含量结果共测定75个样品,其水分含量范围在8.38 % ~11.09 %。
3.3 浸出物含量结果共测定75个样品,其水浸出物含量范围在2.09 % ~7.72 %。
3.4 近红外光谱定量分析模型的建立
3.4.1样品原始光谱图![]()
图3-2 桂枝样品的近红外原始光谱叠加
图3-2为不同批次桂枝样品间的
近红外光谱图,谱图较为相似,近红外原始光谱图与桂皮醛、水分、浸出物含量数据的相关性不显著,故须经过数学处理提取特征信息后,才能建立准确可靠的含量预测模型。
3.4.2样品校正集和验证集划分结果K-S法按照2:1比例对样品进行校正集和验证集划分,选择50个样品用于建立测定桂枝样品中桂皮醛、水分、浸出物含量的定量校正模型,选择25个样品作为验证集,用于验证所建立校正模型的预测能力。校正集和验证集中桂皮醛、水分、浸出物的最大值、最小值和平均值见表3-1。水分、浸出物含量验证集样品包含在校正集中,划分结果可行,有利于建立稳定可靠的模型。
![]()
K-S划分结果,是桂皮醛含量验证集范围超出了校正集,所以用TQ软件自带功能重新对桂皮醛含量模型进行校正集和验证集划分,划分结果见表3-2。
![]()
3.3.3桂皮醛、水分、浸出物含量分析模型建立
(1)桂皮醛定量分析模型建立采用TQ Analyst 9. 1 软件自带化学计量学工具对
近红外光谱进行预处理,消除固体样本颗粒、光散射、杂散光、仪器响应、以及一些与待测样品性质无关的因素所导致的
近红外光谱的基线漂移、噪声等。
考察未处理(None),S-G平滑,ND平滑,一阶导数(FD),二阶导数(SD),多元散射校正(MSC),标准正态变量变换(SNV)以及其组合的预处理方式。
桂皮醛其结构式见图3-3:
![]()
图3-3 桂皮醛结构式
含苯环,为芳烃化合物,芳烃的一级倍频和二级倍频分别在1685 nm(5934 cm
-1)和1143 nm(8749 cm
-1),组合频在2150 nm(4651 cm
-1)和2460 nm(4065 cm
-1)
。
因此,尝试通过手动方法选择不同波段优选建模波段;采用PLS法建立桂皮醛定量校正模型,以校正集样品的以RMSECV、
R2c、RMSEP、
R2p、LVs、Perfformance Index(PI)为指标,优化建模参数。
同过桂皮醛定量模型不同光谱预处理方法的分析,可知:同过PI指数可以看出,MSC处理光谱的效果不如原始光谱、SNV处理光谱的效果优于原始光谱、单独微分处理效果均不如原始光谱,二阶导数效果比一阶更差;MSC、SNV分别与FD、SD组合处理光谱效果均有所提升,与FD的组合模型优化效果更明显;当在此组合基础上再加上平滑处理时建模效果反而下降,说明,平滑的过程可能将有效信息掩盖。最佳光谱预处理组合为:MSC+FD、SNV+FD。光谱经预处理后建模评价参数基本接近,仅有细微差别。因此,暂时将两种处理方式均作为最优预处理方式对待。进行下一步的特征波长优化。
表3-4是MSC+FD、SNV+FD两种预处理方式与不同光谱波段的建模效果
汇总表。从表3-7数据可以看出在用包含芳烃特征吸收的谱段进行建模并没有取得预期的效果,可能与所选取波段不够精准有关系;也可能选取波段使信息量减少,造成了有效信息的丢失;
综合考虑MSC+FD、SNV+FD预处理所建模型评价参数认为SNV+FD更优。
因此,选择SNV+FD预处理方式,全光谱建立PLS最佳模型,模型参数为
R2c=0.9855,
R2p=0.9601,RMSEC=0.0427,RMSEP=0.0487,LVs为5。
![]()
图3-4为桂皮醛预测值与实测值相关图
以PLS法建立的最佳模型计算得到的验证集样品的桂皮醛预测值和UHPLC法测定的结果进行配对t检验,以评价模型的预测能力。表3-3为配对t检验的统计学结果,可见UHPLC测定结果的平均值和NIRS得到的结果均值相同。在95%的置信限下,桂皮醛模型的P=0.451>0.05,说明近红外模型预测的结果和UHPLC的测定结果没有显著性差异,证实了NIRS用于桂枝药材桂皮醛测定的有效性。
![]()
(2)水分定量分析模型建立用Matlab化学计量学分析软件和PLS_Toolbox工具箱对
近红外光谱进行如下步骤的处理和优化,最终建立水分水分定量分析模型。
考察两种常用数据增强算法:均值中心化(Mean Center)、标准化(Autoscaling);
‚考察FD+SG、SD+SG平滑窗口宽度;
ƒ考察MSC、SNV、OSC预处理方式;
④考察FiPLS、BiPLS、以及CARS方法选取特征波段;
⑤采用PLS法建立桂皮醛定量校正模型,以校正集和验证集样品的RMSEC、RMSECV、
R2c、RMSEP、
R2p、LVs为指标,优化建模参数。
⑥采用配对t检验法对预测值与测定值进行差异显著性检验,进一步评价模型准确性。
均值中心化、标准化两种数据增强方式,均优于无处理方式,Mean Center较优,因此在下述处理中mean Center为基础处理方式。
FD+S-G最佳平滑窗口宽度为3,SD+S-G最佳平滑窗口宽度为15,因此在接下来的数据处理中,均以最佳平滑窗口数进行。
通过对不同预处理方式的考察,数据中可以看出最优处理方式为SNV+FD和FD。接下来以SNV+FD、FD分别为光谱预处理方式,进行特征波段选择。
特征波段选择,采用FiPLS和CARS。
预处理方式为FD,FiPLS-300即间隔数为300时,所选的波段区间建模模型RMSEP 最小RMSEC相对较小,
Rc2、
Rp2最大,结果最佳,且变量数最少。
该方法对应光谱区间选择结果如图3-5所示,图形横坐标为波长变量 4000-10000 cm
-1 之间划分的3112个变量顺序,绿色区域对应 RMSECV 最小,即为所选变量区间6527.86-5951.25 cm
-1,共包含300个变量,较全光谱缩减了2812个变量,改善模型结果的同时,降低90%的运算量。
![]()
图 3-5FD,FORWARD iPLS-300 波段选择结果(实验记录Ⅱ-p108)
以CARS法进行变量选择时对模型结果影响较大的两个参数为蒙特卡洛采样次数以及LVs,LVs考察2-10,蒙特卡洛采样次数考察10、25、50、100、200、500,以模型的RMSECV+RMSEP为评价参数。CARS前对图谱进行SNV+FD预处理考察结果见表3-3。
![]()
当LVs为7,采样次数为25时和LVs为8,采样次数为200时RMSECV+RMSEP处在较低水平。因此以这两个参数分别进行CARS波段选择,以FD为预处理方式,进行建模,模型评价见表3-5。
![]()
![]()
![]()
![]()
![]()
最佳建模方式为FD+mean Center,FiPLS-300,模型参数为
R2c=0.964,
R2p=0.962,RMSEC=0.14419,RMSEP=0.13736,LVs为3。图3-10为水分预测值与实测值相关图。
![]()
以PLS法建立的最佳模型计算得到的验证集样品的水分预测值和甲苯法测定的结果进行配对t检验,以评价模型的预测能力。表3-8为配对t检验的统计学结果,可见甲苯测定结果的平均值和NIRS得到的结果均值相同。在95%的置信限下,桂皮醛模型的P=0.56>0.05,说明近红外模型预测的结果和甲苯法的测定结果没有显著性差异,证实了NIRS用于桂枝药材水分测定的有效性。
![]()
(3)浸出物含量定量分析模型建立用Matlab化学计量学分析软件和PLS_Toolbox工具箱对
近红外光谱进行如下步骤的处理和优化,最终建立浸出物含量定量分析模型。
比较两种常用数据增强算法:Mean Center、Autoscaling;考察FD+SG、SD+SG平滑窗口宽度;考察MSC、SNV预处理方式;考察FiPLS、BiPLS方法选取特征波段;采用PLS法建立浸出物定量校正模型,以校正集和验证集样品的RMSEC、RMSECV、
R2c、RMSEP、
R2p、LVs为指标,优化建模参数。
采用配对t检验法对预测值与测定值进行差异显著性检验,进一步评价模型准确性。
![]()
从表3-7知均值中心化(Mean Center)、标准化(Autoscaling)两种数据增强方式,均优于无处理方式,Autoscaling较优,因此在下述处理中Autoscaling为基础处理方式。
表3-8为FD+SG、SD+SG平滑窗口宽度建模效果。由表3-8数据可知,FD+S-G最佳平滑窗口宽度为7,SD+S-G最佳平滑窗口宽度为15,因此在接下来的数据处理中,均以最佳平滑窗口数进行。以下表格中FD、SD均指FD+S-G(7)和SD+S-G(15)。
![]()
![]()
通过对不同预处理方式的考察,在表3-9汇总的数据中可以看出最优处理方式为SNV+SD。以SNV+SD为光谱预处理方式,进行特征波段选择。特征波段选择,采用iPLS。
![]()
![]()
从表3-10可以看出预处理方式为SNV+SD,BiPLS-250即间隔数为250时,所选的波段区间建模模型RMSEP 最小RMSEC相对较小,
Rc2、
Rp2最大,结果最佳。
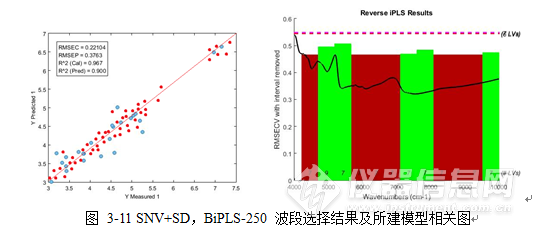
该方法对应光谱区间选择结果如图3-11所示,图形横坐标为波长变量 4000-10000 cm
-1 之间划分的3112个变量顺序,绿色区域对应 RMSECV 最小,即为所选变量区间9999.1-9518.91 cm
-1、8070.63-7108.33 cm
-1、5660.05-4697.75 cm
-1及4213.7-3999.64 cm
-1,共包含1362个变量,较全光谱缩减了1750个变量,改善模型结果的同时,降低56%的运算量。
![]()
![]()
浸出物最佳建模方式为SNV+SD+Autoscaling,BiPLS-250,模型参数为
R2c=0.967,
R2p=0.900,RMSEC=0.22104,RMSEP=0.3763,LVs为3。图3-10为浸出物预测值与实测值相关图。
以PLS法建立的最佳模型计算得到的验证集样品的浸出物预测值和药典法测定的结果进行配对t检验,以评价模型的预测能力。表3-11为配对t检验的统计学结果,可见药典法测定结果的平均值和NIRS得到的结果均值相同。在95%的置信限下,桂皮醛模型的P=0.24>0.05,说明近红外模型预测的结果和药典法的测定结果没有显著性差异,证实了NIRS用于桂枝药材浸出物测定的有效性。
![]()
4总结通过收集市场上不同批次的桂枝样品,用常规方法测定桂皮醛、浸出物和水分的含量。桂皮醛、浸出物和水分的含量范围分别在0.543% ~1.83%、2.09% ~7.72 %和8.38 % ~11.09 %。药典规定桂皮醛、浸出物和水分的合格限为大于等于1.0%、大于等于6.0 %(作为参考)和不得过12 %。可见,市场上桂枝水分含量也基本稳定,而桂皮醛则存在不合格现象。不合格批次33批,占比44 %以上。说明市场上桂枝的品质存在很大的问题,这些与桂枝的产地、采收时间、加工方式不无关系,因此对于入库验收、对投料比例的把握就会提出更加严格的要求,光靠传统经验显然不足,常规方法又费时费力。开发快检方法尤为迫切。
本实验成功运用 Antaris II傅立叶变换
近红外光谱仪以及相关化学计量学软
件和方法建立了桂枝药材中桂皮醛、浸出物和水分的定量分析模型。基于Antaris II
近红外光谱仪的桂枝药材光谱经SNV+SD+Autoscaling,BiPLS-250组合处理,在9999.1-9518.91 cm
-1、8070.63-7108.33 cm
-1、5660.05-4697.75 cm
-1及4213.7-3999.64 cm
-1区间,所建 PLS模型最佳,桂皮醛水分最佳PLS模型参数为
R2c=0.9855,
R2p=0.9601,RMSEC=0.0427,RMSEP=0.0487,LVs为5;水分最佳PLS模型参数为
R2c=0.964,
R2p=0.962,RMSEC=0.14419,RMSEP=0.13736,LVs为3;浸出物最佳PLS模型参数为
R2c=0.967,
R2p=0.900,RMSEC=0.22104,RMSEP=0.3763,LVs为3。为桂枝药材的购买、筛选提供参考方法,保障投料稳定均一,从源头保障产品质量。