维权声明:本文为gunf1987原创作品,本作者与仪器信息网是该作品合法使用者,该作品暂不对外授权转载。其他任何网站、组织、单位或个人等将该作品在本站以外的任何媒体任何形式出现均属侵权违法行为,我们将追究法律责任。
对《水和废水监测分析方法(第四版)》中氯化物测定方法的解读
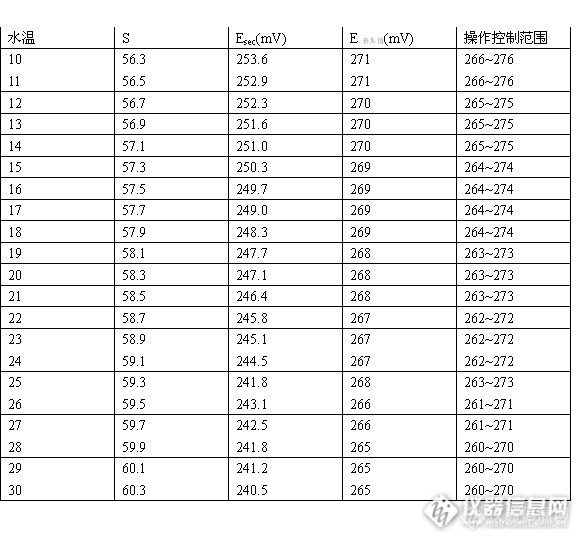
对于氯化物的测定《水和废水监测分析方法(第四版)》中规定硝酸银滴定法为A法,电位滴定、离子色谱、离子选择电极为B法,本文对电位滴定法做初步解读,并和A法做同一样品的同时测定。1对《水和废水监测分析方法》中电位滴定法的初步解析1-1、《水和废水监测分析方法》中电位滴定法的资料来源于《水质分析法》,其中239页图23电位滴定曲线原始点采用“O”标记,”O”的纵向直径代表该点的电位误差,横向直径代表该点的体积误差,而《水和废水监测分析方法》中图3-2-6微分滴定曲线示意图采用“X”标记,没有误差表示。1-2、在《水和废水监测分析方法》和《水质分析法》中的电位滴定法可操作性较差,不能精确计算终点电位和终点体积,目前数码显示的毫伏计已广泛使用,在《分析化学习题集》234页、《分析化学》98页和《化验员读本仪器分析》80-81页均可以准确求出滴定终点时消耗的体积和终点电位毫伏值,因此充分利用现有条件得到更加精确的实验结果已是大势所趋。1-3、终点电位值理论计算E表读数=EAg/Ag+-Esec (1)EAg/Ag+=E0+S*lgCAg+ (2)其中25℃下的E0=799.1 mV, 氯化银的溶度积为1.8*10-10,终点时Ag+的浓度为1.34*10-5mol/L,S=2.303RT/(nF) (R=8.314,n=1,F=96497,T为K氏温度)带入(1)式得到E表读数=799-Esec-4.873*S,因此各种温度下E理论值可求,见下表:![]()
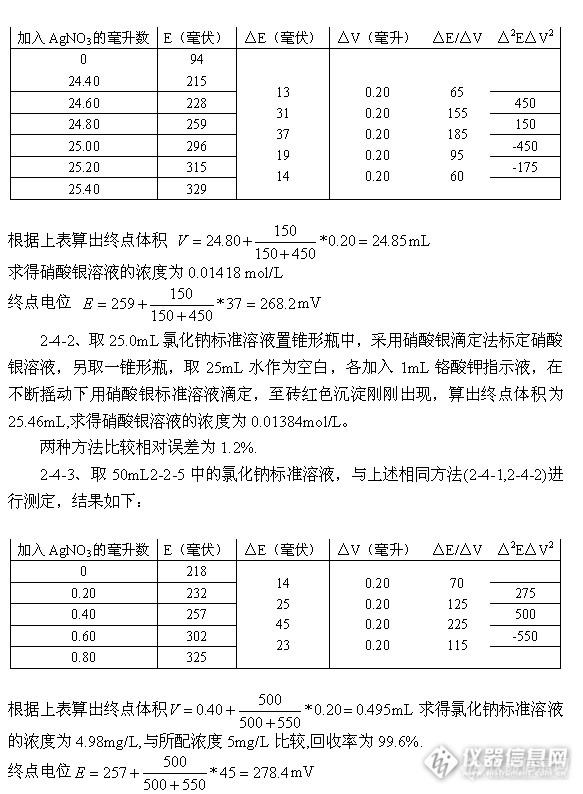
2对比实验部分2-1、仪器和电极2-1-1、仪器:pH计(在mV档使用)2-1-2、电极参比电极:甘汞217型,下端盐桥用过饱和硝酸钾溶液指示电极:216银电极2-2、试剂2-2-1氯化钠标准溶液(NaCl=0.0141mol/L):将基准试剂氯化钠置于坩埚内,在500~600℃加热40~50min。冷却后城区8.2400g溶于蒸馏水中,置1000mL容量瓶中,用水稀释至标线。吸取10.0mL,用水定容至100mL,此溶液每毫升含0.500mg氯化物(Cl-)。2-2-2硝酸银标准溶液(AgNO3≈0.0141mol/L):城区2.395g硝酸银,溶于蒸馏水并稀释至1000ml,贮存于棕色瓶中。用氯化钠标准溶液标定其准确浓度。2-2-3铬酸钾指示液:称取5g铬酸钾溶于少量水中,滴加上述硝酸银至有红色沉淀生成,摇匀,静置12h,然后过滤并用水将过滤液稀释至100ml。2-2-4硝酸(1+3)2-2-5将2-2-1氯化钠标准溶液稀释100倍2-3、电极活化活化电极的目的是形成双电层,使用前用细砂纸将银电极打磨至银白色,在蒸馏水中滴入一滴硝酸或者硝酸银溶液,使毫伏计数值达到280mV以上。2-4、样品测定2-4-1、取25.0mL氯化钠标准溶液于烧杯中,采用电位滴定法标定硝酸银溶液,记录随着硝酸银的滴加电位计的变化,如下表:![]() 3分析与讨论3-1、电位滴定法中只有一个反应:Ag++Cl-=AgCl,而硝酸银滴定法中有两个反应Ag++Cl-=AgCl 、Ag++CrO42-=Ag2CrO4,两个反应同时进行,互相争抢Ag+。3-2、当氯离子含量较高时,两种方法测得结果相差不大,但当氯离子含量较低时,硝酸银滴定法很难操作,两种方法差距很大。3-3、对于初学者而言,硝酸银滴定法判断终点比较困难,需要一定的经验积累,而电位滴定法容易掌握。3-4、对于控制分析,不必每次求导确定终点,只需达到理论电位值即可。参考文献[1]国家环境保护总局.水和废水监测分析方法(第四版).中国环境科学出版社,2002[2]彭图治.分析化学手册(第四分册).化学工业出版社,1999[3]刘珍.化验员读本仪器分析.化学工业出版社,1983 [4]浙江大学分析化学教研组.分析化学习题集.人民教育出版社,1980[5]水质分析法.人民卫生出版社[6]四川大学工科基础化学教学中心.分析化学.科学出版社,2001
3分析与讨论3-1、电位滴定法中只有一个反应:Ag++Cl-=AgCl,而硝酸银滴定法中有两个反应Ag++Cl-=AgCl 、Ag++CrO42-=Ag2CrO4,两个反应同时进行,互相争抢Ag+。3-2、当氯离子含量较高时,两种方法测得结果相差不大,但当氯离子含量较低时,硝酸银滴定法很难操作,两种方法差距很大。3-3、对于初学者而言,硝酸银滴定法判断终点比较困难,需要一定的经验积累,而电位滴定法容易掌握。3-4、对于控制分析,不必每次求导确定终点,只需达到理论电位值即可。参考文献[1]国家环境保护总局.水和废水监测分析方法(第四版).中国环境科学出版社,2002[2]彭图治.分析化学手册(第四分册).化学工业出版社,1999[3]刘珍.化验员读本仪器分析.化学工业出版社,1983 [4]浙江大学分析化学教研组.分析化学习题集.人民教育出版社,1980[5]水质分析法.人民卫生出版社[6]四川大学工科基础化学教学中心.分析化学.科学出版社,2001