维权声明:本文为nphfm2009原创作品,本作者与仪器信息网是该作品合法使用者,该作品暂不对外授权转载。其他任何网站、组织、单位或个人等将该作品在本站以外的任何媒体任何形式出现均属侵权违法行为,我们将追究法律责任。
工业氢氟酸中HF含量的测定(检验报告质量的研判)
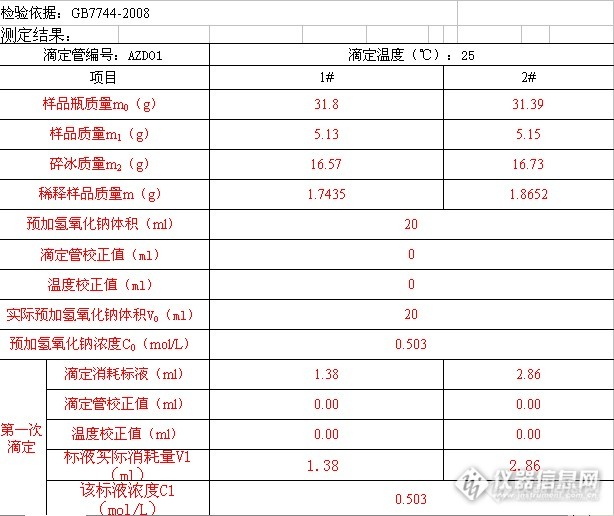
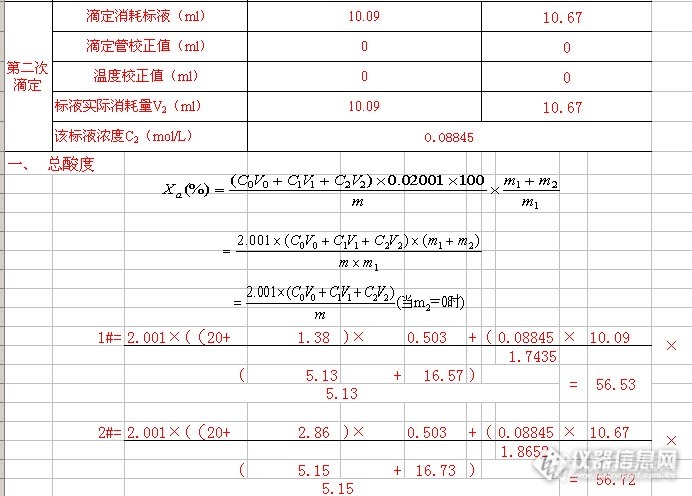
很幸运,这次让我也参加了检验报告质量的研判,就是查看别人的检验报告是否存在问题,这次我查看了工业氢氟酸的检验报告。将两份记录贴上来:![]()
![]()
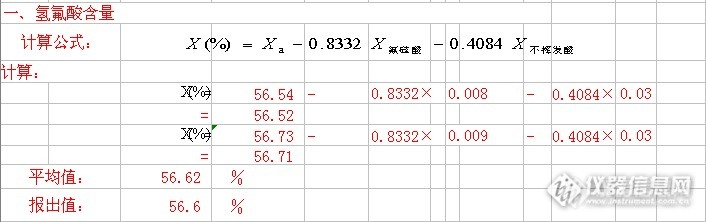
![]() 其中氟硅酸含量
其中氟硅酸含量0.008%
是依据GB7744-2008
硅钼蓝法分光光度法测定得到的(记录略)。大家看到这样一份检验原始记录后,能发现出问题来吗?首先从总酸度的测定原理开始说起:标准是这样写的:
![]() 原理:这其实是氟硅酸钾容量滴定法,确切的说应该是氟硅酸钾沉淀分离—酸碱滴定法。在饱和硝酸钾存在下,可溶性硅酸盐在大量钾离子及
原理:这其实是氟硅酸钾容量滴定法,确切的说应该是氟硅酸钾沉淀分离—酸碱滴定法。在饱和硝酸钾存在下,可溶性硅酸盐在大量钾离子及F-
存在下定量生成氟硅酸钾(K2SiF6)
沉淀。氟硅酸钾在沸水中分解析出氢氟酸(HF)
,以氢氧化钠溶液滴定。主要反应:H2SiF6(氟硅酸)+2K+=K2SiF6↓+2H+ (氢氟酸介质)………(1)
K2SiF6↓+3H2O = 4HF+H2SiO3+2KF (加热水解)……………(2)
HF +NaOH = NaF+H2O ……………(3)
因此结合标准中的操作,应该是这样的,在硝酸钾存在下,以酚酞作指示剂,用氢氧化钠标准溶液滴定用冰冷却的试液。然后再加热并继续滴定。第一次滴定(预加的+V1mL
(记录))相当于除氟硅酸以外的酸以及沉淀氟硅酸时所释放的两个摩尔的酸(见反应式(1
及3
))。第二次滴定(V2
(记录))相当于沉淀的氟硅酸钾加热水解后释放的其余四个摩尔的酸(见反应式(2
及3
))。注意点: 1
)由氟硅酸钾生成的反应看到:SiO32-+2K++6F-+6H+=K2SiF6
↓+3H2O
欲使该反应进行到底,
得到完全的氟硅酸钾沉淀,K+
、F-
、H+
的浓度要有足够。2
)温度也是不可忽视的,在饱和硝酸钾溶液中,只有在室温<35
℃的条件下可生成完全的氟硅酸钾沉淀,温度高于35
℃氟硅酸钾沉淀会不完全或复溶,故要预先加热冰块以冷却滴定的样液。回到检查的记录上来:记录显示第二次滴定(V2
)(第二次滴定V2
消耗0
。1moL/L
的碱用量约10mL
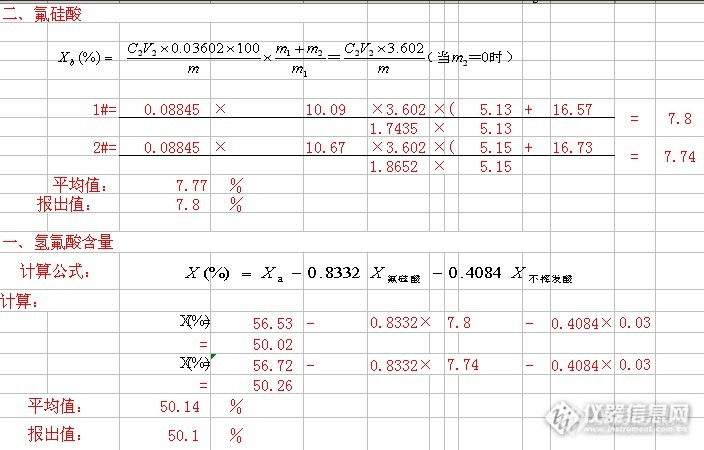
),计算出来氟酸硅与氢氟酸的含量则应该为:![]() 可见氟硅酸含量及氢氟酸含量之差别了(主要是由于氟硅酸含量的差异引起的,由滴定法氟硅酸的含量为
可见氟硅酸含量及氢氟酸含量之差别了(主要是由于氟硅酸含量的差异引起的,由滴定法氟硅酸的含量为7
。8%
,而由硅钼蓝法的则是0
。008%
,同一份样品,这两个测定结果肯定是存在问题的,相对来说硅钼蓝法测得的结果准确些,因此我认为滴定法这个试验过程就存在着问题了,如果V2
的用量这么大(约10mL
)的话,则应该是第一次滴定时会有明显的絮状沉淀物的,否则就是第一次滴定没有真正滴定到终点,剩余的酸留到第二次来滴定。结论:通过这次检验报告质量的研判,也我也进一步明白了工业氢氟酸标准中氢氟酸含量的测定原理,化学分析检验员不仅仅是只会对着标准进行操作,更要明白其中的实验原理,这样才能更好地完成检验工作。