兴奋剂类分析方法系列讲座(10)-GC-MS 测8种β-兴奋剂 气相色谱一质谱法同时测定动物性食品中
8 种β-兴奋剂的残留量
摘 要
目的:应用 OasisMCX 固相萃取净化、
气相色谱-质谱同时测定动物组织样品中8种 β一兴奋剂(克伦特罗、沙丁胺醇、妥布特罗、特布它林、喷布特罗、心得安、倍他索洛尔、非诺特罗)的残留量。
方法:样品粉碎后经β一葡萄糖醛苷酶水解用乙酸钠缓冲溶液提取 MCX 固相萃取柱进一
步净化,再用 N , 0 双(三甲基硅基)三氟乙酰胺一三甲基氯硅烷(BSTFA十TMCA,99十 l )
衍生化,用美托洛尔(metopiobl 为内标。采用选择离子监控模式( SM )检测,GC-MS测定分析,
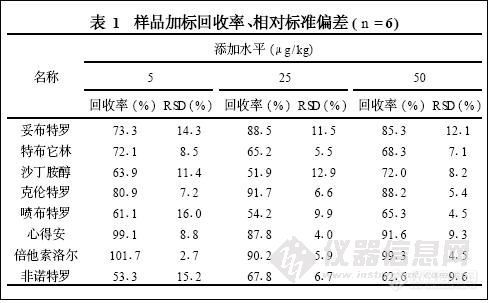
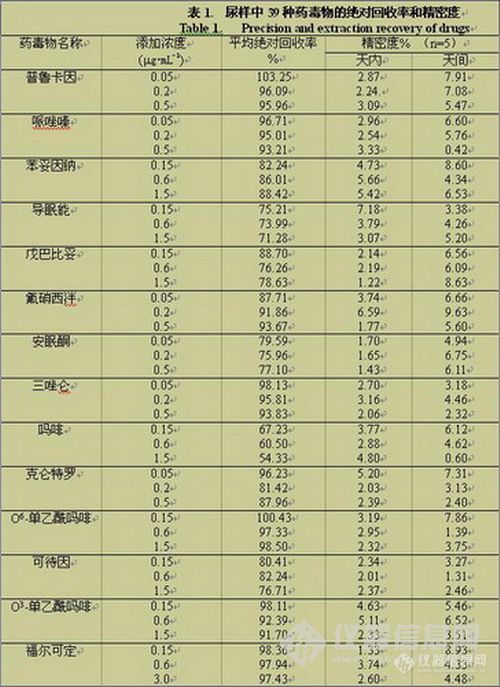
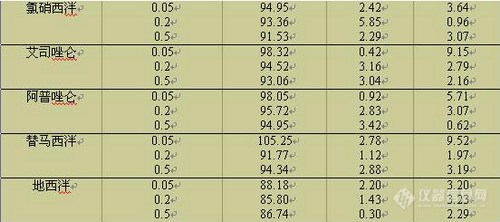
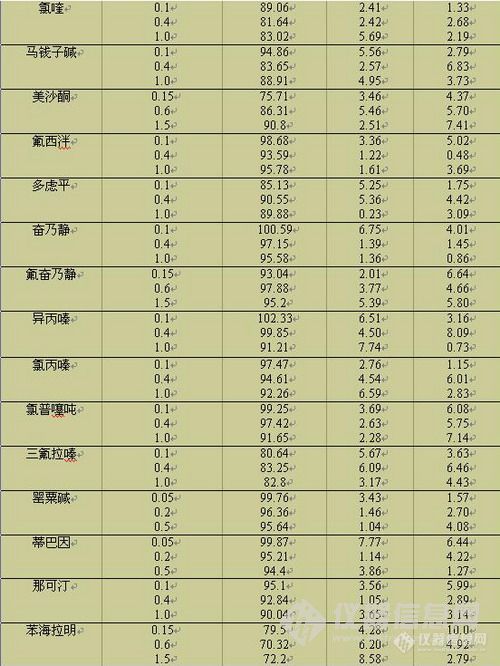
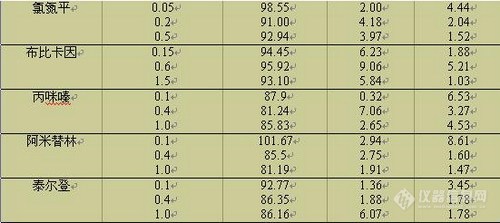
结果:8种β-兴奋剂不同水平的加标:回收率范围为 51 . 9 % ~101 . 7 % ( n = 6 )相对标准偏差为 2 . 7 %~16 . 0 % (n= 6 ) ,
结论:本方法操作筒单.灵敏度高,选择性和重复性好。
本文是北京市自然科学基金资助项目,由北京市疾病预防控制中心的孟娟,邵兵、吴国华、薛颖等研究人员共同完成,为2008年奥运会中兴奋剂的检测有一定参考意义。现全文介绍如下。
前 言
β-兴奋剂(属于苯胺类和苯酚类药物)是一种可以引起交感神经兴奋的类似肾上腺素的药物,被广泛应用于人类哮喘和心脏病的治疗,在高于治疗剂量长期服用时可使体内的营养成分由脂肪组织向肌肉组织转化,提高饲养动物的瘦肉率,但是激素类药物存在着潜在的生理毒性,人长期食用会出现头痛、胸闷、神经过敏、肌肉痛、心悸、恶心等症状。因此其使用受到国际社会的严格限制,β一兴奋剂类药物残留的检测技术多集中在克伦特罗苯胺类单一成分的测定上,现在人们更多致力于探索同时测定多组分β一兴奋剂的方法。
本文应用GC-MS 同时测定动物性织织中 8种β-兴奋剂类药物[克伦特罗、沙丁胺醉、妥布特罗、特布它林、喷布特罗、心得安、倍他索洛尔、非诺特罗的残留量,对前处理的关键步骤进行了多种处理方法的比较,讨论了衍生化时间、洗脱剂的选择、样品过柱前 pH 的选择等.最后对方法进行了优化处理,得出了理想的实验结果。
实 验
l 材料与方法
1 . 1 试剂与仪器
妥布特罗、沙丁胺醇、非诺特罗、特布它林、克伦特罗、喷布特罗、心得安、倍他索洛尔、美托洛尔(sigma公司.纯度 >99%);衍生剂: N , 0 一双甲基硅烷三氟乙酰胺( BSTFA) ;甲醉,乙醇、甲苯均为色谱纯;浓氮水为分析纯;OasisMCX 固相萃取小柱( 500 mg . 3cc , waters 公司):混合型的固相萃取柱,其有反相和阳离子交换的功能: HP -5ms
气相色谱柱( 30m×0.25mm×0.25μm )超声波清洗仪;酸度汁;离心机; 24 位固相萃取仪(Waters公司) ; 6890
气相色谱一 5973 质谱联用仪
( Agilent 公司)。
1 . 2 样品处理
将动物组织样品切碎混匀.准确称取 5.0g,置于 50 ml 离心管中,加入 50 μL β一葡萄糖醛苷酶,再加入 20 ml pH 5 . 2 的乙酸钠缓冲溶液.添加 100ng美托洛尔内标,涡旋混匀, 50 ℃ ±2℃ 孵育 2 h。冷却后加入 0 . 1 mo1/L 高氯酸 10 ml 于超声波清洗器超声 30 min ,再 80 ℃ 水浴 30min,冷却后,于 5000r/min离心 5min 。上清液转移到另一离心管中.再加入 5 mL高氧酸溶解残渣.离心,合并两次上清液用 NaOH ( 0 . 1 mol/L )调 pH 为 3 . 0 ,以 5 000 r/min离心,将上清液全部过柱.。OasisMCX 固相萃取小柱 〔 500mg : 3cc)依次用 6 ml 甲醇 6 ml超纯水活化,将提取液以 lml/min 速度通过固相萃取小柱.再依次用 2 mL 0.lmoL/L 高氯酸、 2 ml 甲醇、 2 ml 水、 25 %甲醇水中含 5 %氨水洗涤固相萃取柱以去除中性杂质,弃去洗涤液,用 6 ml 含有 5 %氨水的乙醇溶液淋洗.收集淋出液,在微弱氮气流下吹至近干。
1 . 3 衍生
将吹干的样品残楂中加入 BSTFA 100 μL密闭,充分涡旋混匀后.置 75 ℃ ±5 ℃ 烘箱中,衍生 30 min.凉置室温后用氮气吹干再加入 1 . 0 mL 甲苯充分溶解,即可上机测定。 1 . 4
气相色谱一质谱测定
色谱条件:毛细管柱 Hp 一5ms色谱柱.柱温条件为:100 ℃ 保持 1 min .以 30 ℃/min升到 190 ℃ ,再以15 ℃ /min 的速度升至 225 ℃ 并保持 5min.再以 30 ℃/min的速度升至 300 ℃ 并保持 5 min .载气: He 流速: 1 . 2 ml/min ;进样口温度: 260 ℃ ,不分流进样,进样量1μL 。
质谱条件:电子轰击(E I)离子源,电子能量: 70eV;扫描范围: 50~500 (m/z ) ,接口温度: 230 ℃ ,倍增器电压:12OV ;N IST107谱库,样品的定量测定采用选择离子模式以多点校正定量,妥布特罗的特征离子为 86 ,194 ,228 ,克伦特罗的特征离子为 86,187 ,243 。喷布特罗的特征离子为 86 , 101 . 247 ,348 .心得安的特征离子为 72 , 115 , 144 ,215 , 倍他索洛尔的特证离子为72, 101 ,263,364 。特布它林的特征离子为 356 , 86 . 426 。沙 丁醇胺的特征离子为 369 , 86 , 350 ,非诺特罗的特征离子为 322 , 356 . 236 .
2 结果与讨论
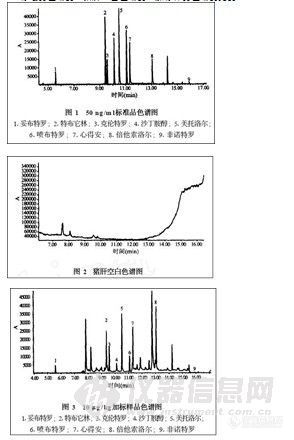
2 . 1 色谱图
标准品色谱图、猪肝空白色谱图、加标样品色谱图见图1~ 3 。
![]()