维权声明:本文为yqfxy原创作品,本作者与仪器信息网是该作品合法使用者,该作品暂不对外授权转载。其他任何网站、组织、单位或个人等将该作品在本站以外的任何媒体任何形式出现均属侵权违法行为,我们将追究法律责任。
1、分析背景:
特殊医学用途全营养配方食品按照GB 5009.82-2016《食品安全国家标准 食品中维生素 A、D、E的测定》第一法 食品中维生素A
和维生素E的测定 反相高效液相色谱法检测维生素E含量。GB 29923-2013要求成品应检测维生素E(α-TE)含量。GB 14880-2012要求维生素E与维生素E(α-TE)转换时,应带入系数进行折算。对产品维生素E与维生素E(α-TE)检验结果进行分析。2、检验方法分析2.1、实验过程使用Sigma生产的α-生育酚(C29H50O2)标准品,CAS号为10191-41-0,标准溶液配制、样品前处理过程,均符合GB 5009.82-2016的要求。2.2、按照GB 5009.82-2016中(6)分析结果的表述,检测结果为试样中的维生素E含量。如维生素E的测定结果要用α-生育酚当量(α-TE)表示,按照维生素E(mgα-TE/100g)=α-生育酚 (mg/100g)+β-生育酚(mg/100g)×0.5+γ-生育酚(mg/100g)×0.1+δ-生育酚(mg/100g)×0.01。润能产品中维生素E来源于食品营养强化剂dl-α-醋酸生育酚,符合GB 14756-2010的规定。产品中不含有β-生育酚、γ-生育酚、δ-生育酚。
3
、操作方法3.1
、结果精密度:在重复性条件下获得的两次独立测定结果的绝对差值不得超过算术平均值的10%。
仪器与用具:高效液相色谱仪、电子天平、紫外可见分光光度计、隔膜真空泵、溶剂过滤器、恒温振荡器、旋转蒸发器、平底烧瓶、量筒、分液漏斗、pH试纸(pH范围1~14)、滤纸、漏斗、旋转蒸发瓶、滴管、容量瓶、移液管、刻度吸管、氮吹仪、0.22μm有机系滤膜。3.2
、试剂:甲醇(色谱纯)、无水乙醇、抗坏血酸、氢氧化钾溶液(50g/100g)、石油醚(30℃~60℃)、无水硫酸钠、2,6-二叔丁基对甲酚(BHT)。
氢氧化钾溶液(50g/100g):称取50g氢氧化钾,加入50mL水溶解,冷却后,储存于聚乙烯瓶中。
3.3
、色谱参考条件:色谱柱:C18柱(柱长250mm,内径4.6mm,粒径5μm),或相当者;柱温:30℃;流动相:甲醇;流速:0.8mL/min;紫外检测波长:维生素A为325nm;维生素E为294nm。3.4、标准溶液配制:标准储备溶液配制:维生素A标准储备溶液(0.500mg/mL):准确称取25.0mg维生素A标准品,用无水乙醇溶解后,转移入50mL容量瓶中,定容至刻度,此溶液浓度约为0.500mg/mL(或同等配制成浓度为0.500mg/mL的维生素A标准储备溶液)。将溶液转移至棕色试剂瓶中,密封后,在-20℃下避光保存,有效期1个月。临用前将溶液回温至20℃,并进行浓度校正。标准储备溶液配制:维生素E标准储备溶液(1.00mg/mL):准确称取α-生育酚50.0mg,用无水乙醇溶解后,转移入50mL容量瓶中,定容至刻度,此溶液浓度约为1.00mg/mL(或同等配制成浓度为1.00mg/mL的维生素E标准储备溶液)。将溶液转移至棕色试剂瓶中,密封后,在-20℃下避光保存,有效期6个月。临用前将溶液回温至20℃,并进行浓度校正。标准储备溶液的浓度校正方法:维生素A的校正:取维生素A标准储备溶液50μL于10mL的棕色容量瓶中,用无水乙醇定容至刻度,混匀,用1cm石英比色杯,以无水乙醇为空白参比,测定其吸光度。维生素E的校正:取维生素E标准储备溶液500μL于10mL棕色容量瓶中,用无水乙醇定容至刻度,混匀,用1cm石英比色杯,以无水乙醇为空白参比,测定其吸光度。试液中维生素A或维生素E的浓度按下式计算:
式中:X——维生素标准稀释液浓度,μg/mL;A——维生素稀释液的平均紫外吸光值;104——换算系数;E——维生素1%比色光系数。
3.5、维生素A和维生素E混合标准溶液中间液:准确吸取维生素A标准储备溶液1.00mL和维生素E标准储备溶液5.00mL于同一50mL容量瓶中,用甲醇定容至刻度,此溶液中维生素A浓度为10.0μg/mL,维生素E浓度为100μg/mL。维生素A和维生素E标准系列工作溶液:分别准确吸取维生素A和维生素E混合标准溶液中间液0.20mL、0.50mL、1.00mL、2.00mL、4.00mL、6.00mL于10mL棕色容量瓶中,用甲醇定容至刻度,该标准系列中维生素A浓度为0.20μg/mL、0.50μg/mL、1.00μg/mL、2.00μg/mL、4.00μg/mL、6.00μg/mL,维生素E浓度为2.00μg/mL、5.00μg/mL、10.0μg/mL、20.0μg/mL、40.0μg/mL、60.0μg/mL。临用前配制。3.6、试样制备:称取50g(精确至0.01g)试样于150mL平底烧瓶中,再加入1.0g抗坏血酸和0.1gBHT,混匀,加入30mL无水乙醇,加入10mL~20mL氢氧化钾溶液,边加边振摇,混匀后于80℃恒温水浴震荡皂化40min,皂化后立即用冷水冷却至室温。(注:皂化时间一般为30min,如皂化液冷却后,液面有浮油,需要加入适量氢氧化钾溶液,并适当延长皂化时间)将皂化液用30mL水转入250mL的分液漏斗中,加入50mL石油醚(30~60℃),振荡萃取5min,将下层溶液转移至另一250mL的分液漏斗中,加入50mL的石油醚(30~60℃)再次萃取,合并醚层。用约100mL水洗涤醚层,约需重复3次,直至将醚层洗至中性(可用pH试纸检测下层溶液pH值),去除下层水相。将洗涤后的醚层经无水硫酸钠(约3g)滤入250mL旋转蒸发瓶中,用约15mL石油醚冲洗分液漏斗及无水硫酸钠2次,并入蒸发瓶内,并将其接在旋转蒸发器上,于40℃水浴中减压蒸馏,待瓶中醚液剩下约2mL时,取下蒸发瓶,立即用氮气吹至近干。用甲醇分次将蒸发瓶中残留物溶解并转移至50mL容量瓶中,定容至刻度。溶液过0.22μm有机系滤膜后供高效液相色谱测定。
3.7
、标准曲线的制作:将维生素A和维生素E标准系列工作溶液分别以20μL注入高效液相色谱仪中,测定相应的峰面积,以峰面积为纵坐标,以标准测定液浓度为横坐标绘制标准曲线,计算直线回归方程。
3.8、
样品测定:将试样溶液20μL注入高效液相色谱仪进行分析,测得峰面积,采用外标法计算。
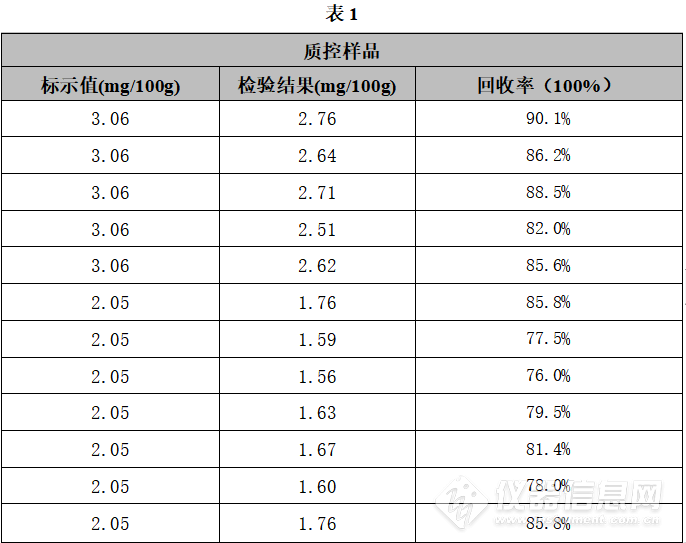
3.9、结果精密度:在重复性条件下获得的两次独立测定结果的绝对差值不得超过算术平均值的10%。4.检验结果如下表(因为本次是对特医食品的首次操作,且产品里面的配方内容较多,综合因素,本次使用了质控样品进行检测)
![]()
5.数据分析
现在看维生素E的检验结果回收率在77.5%-90.1%之间。维生素E本身是脂溶性维生素,按照原料厂家给出的建议,容易分解。按照购买的标准物质的标示值的要求,检验结果应在标示值的70%-120%之间。检验结果合格。
6.心得总结
这是首次常识在特医食品中加入标准品,做回收率。在检测过程中由于特医食品里面的配方复杂,且状态又是混悬的,所以给检验人员很大的挑战。最总的加标选择了,先称量样品,然后在添加标准品的方式进行。也考虑到如果先在样品中加入标准品,然后在称量。那由于标准品不能很好的分散在样品里面,取样时不能具有代表性。
另外样品在加入抗坏血酸和BKT都是为了防止脂溶性维生素氧化,所以觉得两个抗氧剂的用量没必要太纠结。加多了对结果也不会产生影响。