[电化学专题]:电 动 势 测 定
背景知识
一、关于电池、电极和盐桥
电化学是研究电现象与化学现象之间内在联系的一门学科,其最基本的要素是电极和溶液。电极能传导电子,常为金属,也可以是半导体。电池是原电池和电解池的通称,电池由至少两个电极及相应的电解质组成,它依靠离子导电,通常是水溶液,也可以是非水溶液、熔盐或固体电解质。
1、电极反应:在电极-溶液界面上产生的伴有电子得失的氧化或还原反应。
2、电池反应:电池中各个电极反应、其它界面上的变化以及由离子迁移所引起的变化的总合。其中必进行氧化还原反应。
3、阳极:负离子趋向或正离子离开的电极。在阳极上产生失电子的氧化反应,电流由电极进入溶液。
4、阴极:正离子趋向或负离子离开的电极。在阴极上产生得电子的还原反应,电流由溶液进入电极。
5、正极:电势高的电极。
6、负极:电势低的电极。
7、原电池:将化学能转变为电能的装置,池内发生 0的自发反应,运行时两电极间产生的电势差形成了对外做功(输出电能)的本领。又称之为伽伐尼电池。
8、电解池:将电能转化为化学能的装置,池内发生 0的非自发反应,运行时电池消耗从外界输入的电能。
当通过电极的电流为零,电池达到电化学平衡时,原电池与电解池也就没有区别。
9、可逆电池:满足热力学可逆条件的电池,其两端的电势差为该可逆电池的电动势。形象地说,电动势是促使电荷流动的势头。可逆电池须满足以下三个条件:
(1)电极和电池反应本身须可逆,这样在电池充电时,可使放电反应的物质得到复原。
(2)在充或放电过程中,通过电极的电流须无限小,此时电极反应在接近电化学平衡的状态下进行,电池能作最大的非体积功。这样在电池充电时,可使原放电时的能量得到复原。
(3)电池工作时,无其他不可逆过程(如扩散)存在。
10、可逆电极:可逆电池要求其各个相界面上发生的变化都是可逆的,亦即电极/溶液界面上的电极反应同样须是可逆的,此即可逆电极。
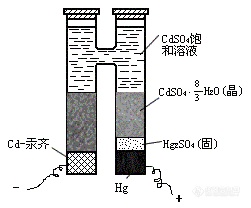
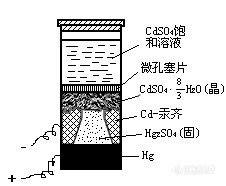
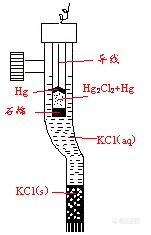
11、标准电池:作为电动势测定时校验之用,它具有稳定的电动势,且其温度系数很小。韦斯顿发明的镉汞电池常作为标准电池,这种电池具有高度可逆性。韦斯顿标准电池多为饱和式,有H管型和单管型两种,如图1所示。对于H型标准电池,负极为镉汞齐(含12.5%Cd),上部铺以CdSO4∙ H2O(s),正极为纯Hg上铺盖糊体状的Hg2SO4(s)和少量CdSO4∙ H2O(s),两极之间盛以CdSO4的饱和溶液,管的顶端须密封,并留一定空间以供热膨胀之用,两极的底部各接一铂丝与电极相连。做标准电池所用的各种物质须极纯。
![]()