3.用0.1mol.L_1HCl滴定20ml 0.1mol.L_1左右的NH3.H2O溶液
当二者恰好中和时,因为产物为水解呈酸性的NH4Cl ,其[OH-]=(C×Kω/Kb)0.5=
(0.05×10-14/1.8×10-5)0.5=5.3×10-6, PH=5.3,用甲基橙为指示剂,当溶液PH<4.4时,
溶液颜色由黄色→橙色,为终点。这时盐酸已过量,同理此时只有千分之二的误差;
若选用酚酞,PH<8时达终点,较之选用甲基橙误差更大,且不符合视觉要求。所以强酸滴定弱碱时必须选用甲基橙(或甲基红);
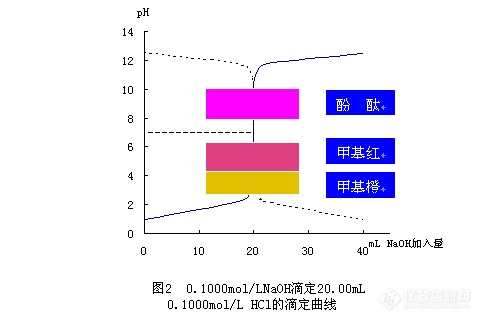
4.同理:若用0.1mol.L_1 NaOH滴定20ml 0.1mol.L_1左右的HAc溶液
当二者恰好中和时,因为产物为水解呈碱性的NaAc ,其[OH-]=(C×Kω/Ka)0.5=
(0.05×10-14/1.8×10-5)0.5=5.3×10-6, POH=5.3,PH=9.7,用酚酞作指示剂,当PH>8时,溶液由无色→红色,,为终点。这时NaOH还差一点,此时的误差更小。若选甲基橙,则终点与指示剂的变色点相差太远,误差会很大,且不符合视觉要求。所以强碱滴定弱酸时,必须选用酚酞。
三、 其它滴定实验中指示剂的选择1.双指示剂法
若有Na2CO3 、NaHCO3(或NaOH、Na2CO3)的混合物。可用标准盐酸选用不同
指示剂进行分步滴定测出二者的含量:
方法:配制一定体积的待测液,用标准盐酸滴定,先加酚酞为指示剂,达终点时,溶液由红色→无色,测得耗盐酸V1,发生反应Na2CO3+ HCl= NaHCO3+NaCl;再向其中加甲基橙,再达终点时,溶液由黄色→橙色,测得耗盐酸V2,发生反应
NaHCO3+ HCl= H2O+CO2↑+NaCl;据V1、V2的关系可求两盐的含量;
2.碘水与还原性溶液的氧化还原反应滴定用碘水与无色的Na2S2O3溶
液相互滴定,反应为2S2O32-+I2= S4O62-+2I-,可用淀
粉为指示剂。当碘滴定Na2S2O3溶液时,溶液由无色→蓝色即达终点;反之溶液由蓝色→无色即达终点。
3.KMnO4溶液与还原性的亚铁盐、草酸等的氧化还原滴定由于KMnO4溶液本身为紫红色的,而亚铁盐、草酸等色浅或无色,不必外加指
示剂,KMnO4溶液本身兼具指示剂的作用,当KMnO4溶液滴定亚铁盐、草酸溶液时,终点为无色→紫红色;反之终点为紫红色→无色。
总之,对于属信息题的氧化还原滴定,若反应中只有一种物质的溶液有特殊明显的颜色,则此有色物本身为指示剂,不必外加指示剂。