维权声明:本文为hhciq原创作品,本作者与仪器信息网是该作品合法使用者,该作品暂不对外授权转载。其他任何网站、组织、单位或个人等将该作品在本站以外的任何媒体任何形式出现均属侵权违法行为,我们将追究法律责任。
离子色谱-抑制电导法快速测定葡萄酒中硫酸根离子
摘 要 :采用离子色谱-抑制性电导检测器方法检测葡萄酒中硫酸根的含量,研究葡萄酒中快速准确的可溶性硫酸盐的检测方法。线性方程Y=0.588 X+0.117,确定系数R2=99.998,线性关系良好。硫酸根的检出限1.0 mg·L-1,相对标准偏差(RSD%)0.16%,加标回收率为96.9%~104.6%。实际检测方法简便、快速、准确。关键词:葡萄酒;硫酸根;离子色谱中图分类号:O 657.7 文献标识码:A 文章编号:Method for the determination of Sulfate ion in Wine—Ion chromatography inhibitory conductance
Abstract:This paper establishes a method for determination of sulfate in wine with ion chromatographyinhibitory conductance.The qualitative and quantitative method is rapid and accurate research in wine. The linear equation is Y=0.588 X+0.117.The coefficient determination is 99.998 and the linear relationship is good.The detection limits of Sulfate ion were 1.0 mg·L-1。The average recovery for sulfate ion was 96.9%~104.6% ,relative standard deviations was 0.16%. The experiment shows that this method could be simple,rapid and accurate.Keyword:Wine;Sulfate ion;Ion chromatography 在化学有害物中,硫酸盐对人类健康可产生严重的影响[1]。目前中国全年葡萄酒产量100万吨,葡萄酒越来越成为重要的新兴产业,其质量对人民健康的影响也越来越大。葡萄酒中的硫酸盐降低了葡萄酒的适口性,影响饮用效果,影响酒石酸的溶解与平衡[2],引起不良的味道和具有腹泻作用[3]。葡萄酒中硫酸盐含量已构成了食品安全问题,对产品质量和饮用者健康的影响不可忽视。
中国法规对于成品葡萄酒中硫酸盐项目的检测方法和限量要求均未涉及[4~7],我国检葡萄酒中硫酸盐检测技术方法的空白,严重制约了葡萄酒在国内和国际市场的发展,也影响了国民身体健康。
目前监测硫酸盐的方法主要有重量法[1,8]、比浊法[9]、火焰原子吸收分光光度法[10]、铬酸钡分光光度法[11]、电感耦合等离子体发射光谱法 [12]、电位法[13]、离子色谱法 [14]、四羟基醌-硫酸钡滴定法[15]、络合滴定法 [16]、流动注射分析法[17]等方法,国际葡萄与葡萄酒组织(O.I.V)的检测方法[1]为钡盐沉淀方法,操作环节多、引入人为误差大,检出限高。
离子色谱-抑制电导法方法检测硫酸根,换算为硫酸盐后,检测指标满足O.I.V对葡萄酒中硫酸盐含量规定的要求[1],前处理方法采用物理分离技术,方法简单、回收率稳定,适用于葡萄酒特别是进出口葡萄酒的检验。
1 材料与方法1.1 材料与试剂硫酸根离子(SO42-)标准工作液:将基准试剂超用纯水溶解并定容,逐步稀释至标准工作液。 100 mmol·L-1的 NaOH溶液。1.2 仪器与设备ICS-3000型离子色谱系统(Dionex公司);ASRS型抑制性电导检测器;OnGuard RP柱、OnGuard Ag柱和OnGuard Na柱(Dionex公司)。分析柱Dionex IonPacAS11-HC(4 mm×250 mm);保护柱IonPacAG11-HC,50*4mm;进样体积:50 μL;流速:1.0 mL·min-1;柱温:30℃;电导检测池温度:35 ℃;淋洗液:洗液组成及流速:NaOH梯度淋洗程序:0 min~26 min,13 m mg·L-1;26 min~35 min,60 m mg·L-1;35.1 min~40 min,13 m mg·L-1;流速1.0 mL·min-1。1.3 方法精确量取试样10 mL,用0.04%甲醛溶液定容至200 mL容量瓶中,涡流振荡器摇匀,溶液于10 000 rpm离心15 min,取上清液过0.22 μm尼龙滤膜和OnGuard RP固相萃取柱(2.5cc),弃初始6 mL滤出液后收集1 mL,供离子色谱仪测定。外标法定量。2 结果与讨论2.1 线性关系及精密度在最佳分离条件下,分别以不同浓度的硫酸根标准工作溶液,以峰面积Y对质量浓度X (mg/L)求得的线性回归方程为:Y=0.588 X+0.117,确定系数R2=99.998,硫酸根在1.0 mg·L-1~50 mg·L-1范围内线性关系良好。确定本方法的硫酸根的检出限为1.0 mg·L-1。标准工作曲线图见图1。![]()
图1. 标准工作曲线图
Fig.1. The chromatogram of standard solution
用浓度为10 mg·L-1的硫酸根标准溶液,在相同条件下,连续进行6次平行测定,考察方法的准确度。表1结果表明。测定结果的相对标准偏差为0.6%,说明方法准确度高。表1. 方法的准确度(n=6)
Tab 1. The accuracy of the method (n=6)
| 测定次数 1 2 3 4 5 6 相对标准偏差(%) |
| 测定值(mg·L-1)9.81 9.88 9.73 9.73 9.79 9.84 0.6 |
2.2 硫酸根的分离
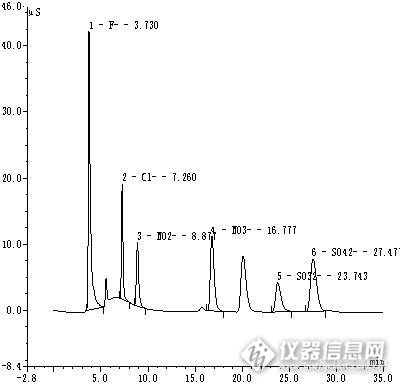
在样品中加入硫酸根标液20 mg·L-1,考察硫酸根的分离度,见图2。常见阴离子对硫酸根的分离没有影响。![]()
图2. 硫酸根的分离效果
Fig.2. The separation effect of sulfate ion
2.3不同浓度的甲醛稳定剂对硫酸根的影响葡萄酒中含有亚硫酸根,可能影响硫酸根的测定。加入甲醛作为稳定剂,可以防止亚硫酸根影响硫酸根的测定。在样液中加入硫酸根标准溶液20 mg·L-1,考察不同浓度的甲醛稳定剂对硫酸根测定的影响。见表2。表2. 不同甲醛浓度对硫酸根的影响(n=6)
Tab 2. Effects of different formaldehyde concentration of sulfate ion
| 甲醛浓度% 0. 00 0.01 0.02 0.04 0.06 0.08 0.12 0.16 |
1 17.9 19.0 17.7 18.6 18.8 18.5 17.7 16.8
2 18.2 18.3 18.3 18.6 19.0 18.5 18.1 17.3
3 17.9 18.6 18.1 20.0 18.5 18.1 18.4 17.6
4 18.3 18.4 18.4 19.6 18.5 17.5 18.4 17.1
5 18.1 18.3 17.7 18.5 19.2 18.3 16.2 17.7
6 17.8 19.3 20.3 18.6 19.0 18.2 18.1 17.2
平均值 18.0 18.7 18.4 19.0 18.8 18.2 17.8 17.3
平均回收率% 90.15 93.25 92.10 94.80 94.15 90.90 89.10 86.40
RSD% 1.09 2.22 5.26 3.40 1.5.3 2.04 4.67 1.92 |
从表2数据结果表明,随甲醛浓度的增加,被测硫酸根的回收率呈缓慢增加,在0.04%浓度附近区域平缓;当甲醛含量超过0.06%时,被测硫酸根的回收率呈平稳趋势。而葡萄酒试样未经添加甲醛稳定剂时,其硫酸根标液回收率达90.4%,与添加甲醛浓度0.04%的葡萄酒样品中硫酸根回收率相比较略低。由此,选择用0.04%浓度的甲醛作为稳定剂。2.4 样品PH值的影响由于葡萄酒含有有机酸,酒液呈酸性;而淋洗液为氢氧化钠体系,呈碱性。二者混合后,柱子中的淋洗液pH值将发生由碱性环境——酸性环境——碱性环境的变化,将干扰淋洗液碱液浓度,同时由于可能产生盐的结晶或沉淀,堵塞色谱柱和管道。同一葡萄酒试样10 mL,添加相同的硫酸根标液20 mg·L-1,加入适量0.04 %甲醛溶液后,用氢氧化钠/盐酸调节样液的pH值,再用0.04 %甲醛溶液定容至200 mL容量瓶中,考察不同pH值对测定结果的影响,结果见表3。表3. 不同pH值的影响(n=6,回收率%)
Tab 3.Effects of different pH(n=6,recovery %)
| 次数 未调节 pH 2 pH 3 pH 5 pH 6 pH 7 pH 8 pH 10 pH 12 |
1 17.8 2.81 8.33 18.0 18.1 18.0 18.4 18.9 23.9
2 18.5 2.69 8.86 18.1 18.4 17.9 18.5 18.9 24.1
3 18.1 3.99 8.75 17.9 18.1 18.1 18.5 18.9 25.6
4 18.3 4.70 9.00 18.3 18.4 18.5 18.7 18.9 25.4
5 18.4 4.68 9.36 18.5 18.4 18.7 19.5 19.0 25.4
6 18.4 4.17 9.62 18.6 18.2 18.3 20.2 18.9 25.4
平均值 18.25 3.84 8.99 18.3 18.3 18.3 19.0 18.9 25.0
回收率%91.3 19.2 45.0 91.2 91.4 91.3 94.9 94.5 124.9
RSD% 1.4 23.2 5.1 1.5 0.8 1.7 3.9 0.2 3.0 |
从表3数据结果表明,随样液pH值的不同,SO42-的回收率不同,在pH值在强酸性条件下,回收率减少;并且用盐酸溶液调节pH后,氯离子其响应值达到600,对目标离子及其他离子干扰较大;在pH值在偏中性和近碱性条件下,回收率均在90%以上,变化较平缓;当pH值超过10,回收率呈增大的趋势。葡萄酒样品自然呈酸性,在调节pH的回收率在91%,并且稳定性较好。所以在实际测定葡萄酒样品中的硫酸根时,pH值如果不是低于5,不用调节。2.5 流动相的选择通过改变NaOH淋洗液浓度,考察NaOH溶液不同浓度对相同样液中硫酸根离子的影响。结果见表4。表4. 不同NaOH淋洗液浓度的影响
Tab 4.Effects of different concentration of NaOH
| 浓度(mmoL·L-1) 4.0 6.0 8.0 10.0 13.0 18.0 |
次数 1 - - - 17.5 18.7 -
2 - - - 17.4 18.8 -
3 - - - 17.0 18.7 -
4 - - - 18.2 18.3 -
5 - - - 17.8 18.4 -
6 - - - 17.9 18.3 -
平均值 0 0 0 17.6 18.5
标准偏差(S) 0.423 0.225
相对平均偏差(%) 1.89 1.08
相对标准偏差(RSD%) 2.4 1.2 |
从表4中试验数据及试验中的色谱图中可以看出,淋洗液NaOH浓度小于10 mmol·L-1时,硫酸根的出峰间推迟太长,并受其他的离子的峰的干扰,严重影响目标峰的分离度,无法对硫酸根离子的峰进行定性;而当淋洗液NaOH浓度大于13 mmol·L-1时,F-的保留时间基本没有变化,Cl-的保留时间有所缩短,但变化较小,而SO42-、SO32-、NO-、PO4-随NaOH溶液浓度的增大保留时间明显缩短;当NaOH溶液的浓度在10 mmol·L-1~13 mmol·L-1时,阴离子分离效果和峰形均较好。所得标准溶液添加回收率(表4)和样品的色谱图(图2)也证明了这一结论。2.6 实际样品的测定在选定的条件下,对市售的葡萄酒进行分析,分析结果见表5、表6。表5. 不同葡萄酒样品中的相对偏差
Tab 5.Relative standard deviations of different wine samples
样品 测定值(mg·L-1) 平均值(mgmg·L-1) 相对标准偏差 1 2 3 |
国产干红 427.46 433.71 437.85 433.0 1.2 澳大利亚干红 348.76 358.32 355.59 354.2 1.4 澳大利亚干白 178.87 178.80 176.70 178.1 0.7 |
表6. 葡萄酒中硫酸盐的回收率
Tab 6.The recovery of sulfate ionin wine sample
| 实验号 本底值(mg·L-1) 添加量(mg·L-1) 测定值(mg·L-1) 回收率% |
1 348.8 350.0 714.9 104.6
2 352.3 350.0 692.6 97.2
3 355.6 350.0 710.1 101.3
4 350.0 350.0 689.1 96.9
5 350.3 350.0 697.5 99.2
6 358.3 350.0 711.2 100.8 |
用同一干红葡萄酒样品2份,一份测定本底,另一份添加一定量硫酸盐标准液,分析并计算硫酸盐的回收率,结果见表6。数据显示加标回收率为96.9%~104.6%。3 结论离子色谱-电导检测器定量检测葡萄酒中可溶性硫酸盐,经试验证明可以较好地分析葡萄酒中可溶性硫酸盐含量。样品处理简单、灵敏度高、速度快、准确,对测定葡萄酒中可溶性硫酸盐有实用价值,填补了国内葡萄酒中可溶性硫酸盐检测方法的空白。参考文献:[1] 国际葡萄与葡萄酒组织.国际葡萄酒与葡萄汁分析方法汇编[M].中国计量出版社,2005,李记明,马佩选,编译.[2] 赵学方,田常余,主编. 生活饮用水卫生管理[M].济南:山东科学技术出版社,1990,27[3] 薛洁.葡萄酒中酒石酸氢钾稳定性[J].中外葡萄与葡萄酒,2002,5:54-55[4] GBT 15038葡萄酒、果酒通用分析方法.中华人民共和国国家质量监督检验检疫总局.北京:中华人民共和国国家质量监督检验检疫总局,2006。[5] GB 15037葡萄酒.中华人民共和国国家质量监督检验检疫总局.北京:中华人民共和国国家质量监督检验检疫总局,2006。[6] CCGF 103.4-2010葡萄酒 产品质量监督抽查实施规范. [中华人民共和国国家质量监督检验检疫总局S].北京:中华人民共和国国家质量监督检验检疫总局,2006[7] GB 2758-2005发酵酒卫生标准.中华人民共和国国家质量监督检验检疫总局.北京:中华人民共和国国家质量监督检验检疫总局,2005。[8] GB/T 11213.5-2006化纤用氢氧化钠中硫酸盐含量的测定 硫酸钡重量法(甲法).中华人民共和国化学工业部.北京:中华人民共和国化学工业部,1988。[9] GB/T 23844-2009 无机化工产品中硫酸盐测定通用方法目视比浊法.中华人民共和国国家质量监督检验检疫总局.北京:中华人民共和国国家质量监督检验检疫总局,2009。[10] GB 13196-91水质硫酸盐的测定火焰原子吸收分光光度法.国家环境保护局.北京:国家环境保护局,1991。[11] HJ/T 342-2007水质硫酸盐的测定 铬酸钡分光光度法.国家环境保护总局.北京:国家环境保护总局,2007。[12]高玲,杨元,谯斌宗,王珅明. 电感耦合等离子体发射光谱法测定水中硫酸盐方法研究[J].中国卫生检验杂志,2008,18(7):1234-1301[13] 李占灵,汪振辉.电位法测定水中硫酸盐方法的研究[J].周口师范学院学报,2005,22(5):71-72[14] Margaret NeaL.CoLin NeaL Determination of bromide,chLoride,nitrate and suLphate by ion chromatography:comparisons of methodoLogies for rainfa LL,cLoud waters atthe PLynLimon catchments of mid WaLes[J].Hydrol EaLth Syst Sci,2007,11(1):294-300.[15] 刘玉凤.四羟基醌-硫酸钡滴定法测定生活饮用水中硫酸盐[J].陕西化工,1999,28(9):30-31[16] 闰仲禹,郭培森,贾秀军.水中硫酸盐和总硬度同时测定的EDTA络合滴定法[J].职业与健康,2003,l9(4):39-40[17]王百文.流动注射分析法测定饮用水中硫酸盐[J].齐齐哈尔医学院学报,2007,28(9):1080-1081