有效期系指市售包装药品在规定的贮存条件下放置,药品的质量仍符合注册质量标准的时间段。药品的有效期应综合加速试验和长期试验的结果,进行适当的统计分析得到,最终有效期的确定一般以长期试验的结果来确定[1]。
但在审评工作中,建立有效期时仍然遇到一些问题。如基于商业需要,生产企业通常希望将有效期订得时间更长,但却往往忽略一些可能影响药品质量和安全性的因素,如较少考虑所销售区域的高温、高湿、强光等特殊气候环境对药物稳定性影响等。本文就确定有效期时需要关注的几点总结如下,供参考。
一、建立有效期的稳定性试验基础应可靠
稳定性试验基础系指加速试验和长期试验的试验设计应合理,样品的批次和规模应符合要求,考察项目应全面且具有灵敏性,各项目的分析方法应经过充分验证,测试试验数据应准确等。没有以上这些试验基础,是无法准确确定有效期的,也就无法保证上市后产品在一定时期内的质量和安全。
例如,某补充申请延长有效期(由24个月至36个月),但所使用的样品批次仍为申请注册上市的中试规模产品,此情形下延长有效期至36个月则欠妥。通常,生产企业应在批准上市后使用大生产规模的批次继续进行长期试验,此时需提供大生产规模稳定性数据才有可能支持36个月有效期。
还有一种较常见的情况是,在建立或延长有效期时,长期试验缺少对有关物质或降解产物等关键指标的考察,此时无法全面评价药物质量随时间的变化,因此无法支持所申请的有效期。
二、应考虑产品销售区域的特定气候的影响
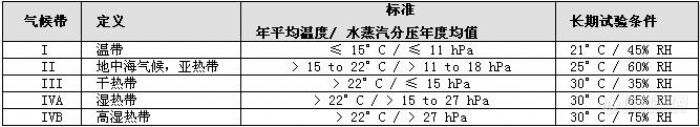
目前,稳定性长期试验所采用的一般条件是根据国际气候带制定的。Paul Schumacher在1972年,Wolfgang Grimm 在1986 和1998年根据国际四个不同气候带定义了四个稳定性长期试验条件,在这四种气候带中,对于药品的质量保证而言,条件最苛刻的是第四种气候带,即高温又高湿的环境。上述作法被一些国家当局所采用并逐渐成为稳定性研究的标准作法。在2005年10月日内瓦举行的WHO关于药物制备规范专家委员会第四次会议上,建议将气候带IV(湿热带)分为 IVA和IVB两个气候带,其中 IVA的长期稳定性条件为30°C/65% RH,IVB为30°C/75% RH。WHO草案推荐的气候带分区和相应的长期稳定性试验条件见下表[2]
![]()