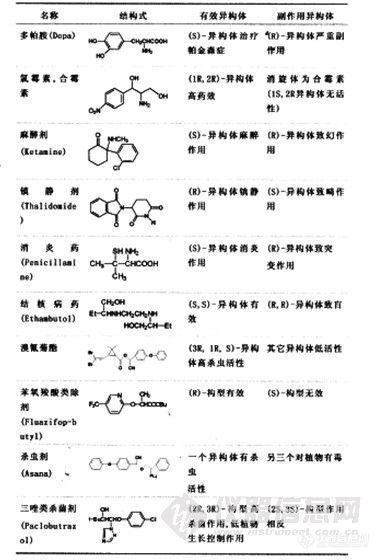
气相色谱手性分离 (6)
. gc 手性固定相的分类按照样品和固定相的作用模式可以把
gc手性固定液分为三类:
1.氢键型
2.配位型(coordination)
3.包含型(inclusion)
(P. Schreier, A. Bernreuther, M. Huffer, Analysis of Chiral Organic Molecules, Walter de Gruyter, Berlin, 1995.,
W.A. Konig, Trends Anal. Chem. 1993,12:130.)
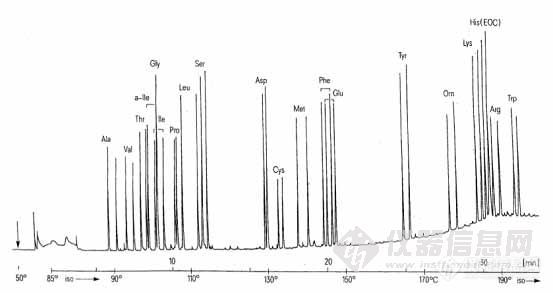
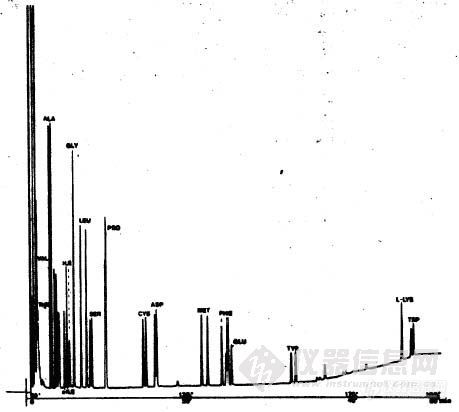
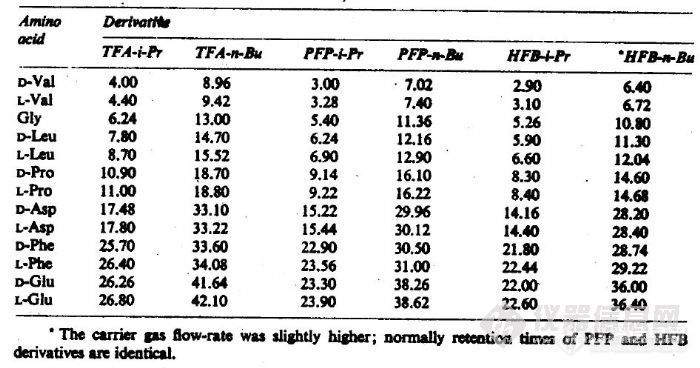
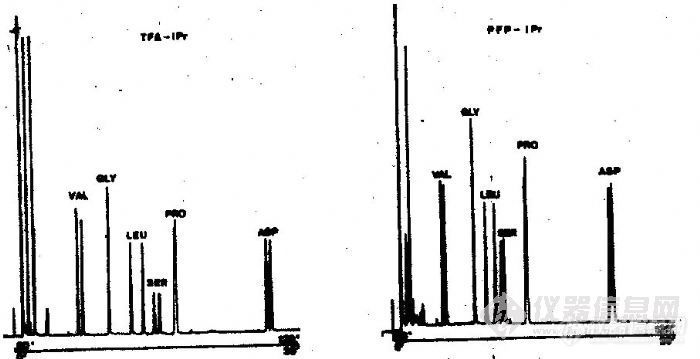
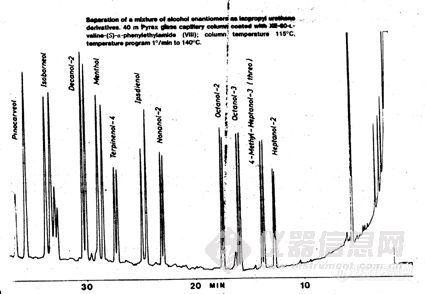
· 利用氢键型作用力在手性氨基酸衍生物固定相上分离氨基酸对映体。
(H. Frank, G.J. Nicholson, E. Bayer, J. Chromatogr. Sci., 1977,15:174.)
· 利用形成配位络合物在配位型固定相上分离金属配位型对映体。
(V. Schurig, J. Chromatogr. 1988,441:135.)
· 利用形成包含化合物在包含型固定相(环糊精衍生物)上分离对映体。
(V. Schurig, J. Chromatogr. A 1994,666:111.)
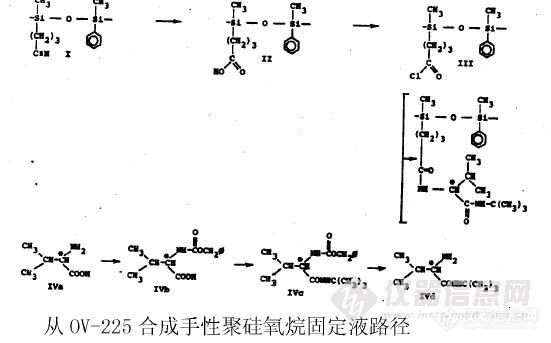
在开始时手性选择剂(固定液)使用纯液体,或者在角鲨烷或聚硅氧烷中的溶液,为了提高色谱柱的柱效和选择性,就把手性选择剂键合到聚硅氧烷链上,变成聚硅氧烷型手性固定相(Chirasil-type),这样一来大大提高了热稳定性、柱效和耐用性。
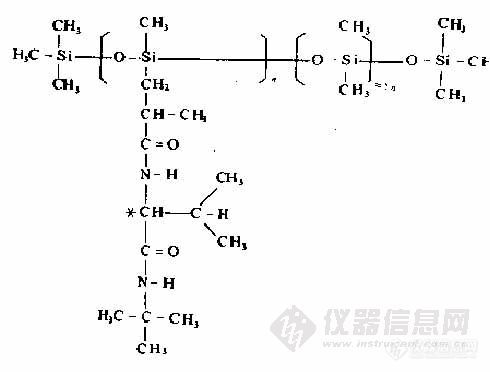
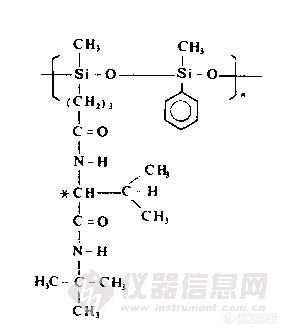
1978年合成了聚合物手性固定液,即把L-缬氨酸-特丁酰胺接枝到聚硅氧烷上,商品名“Chirasil-Val”,见图 6-1 。这一固定液可以使用到 220℃。特别适用于氨基酸手性异构体的分离,对手性胺类、氨基醇类、α-羟基基酸酰胺类的分离。
(Volker Schurig,J.Chromatogr. A, 2001, 906 :275–299)
![]()
图 6-1 “Chirasil-Val” 的结构式