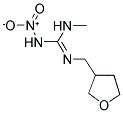
液相色谱-电喷雾电离三级四极杆质谱法测定茶叶中6种烟碱类农药残留
【摘要】 应用
液相色谱²电喷雾电离三级四极杆质谱(LC-ESI-MS/MS)方法测定茶叶中呋虫胺、噻虫嗪、噻虫胺、吡虫啉、啶虫咪和噻虫啉烟碱类农药残留。前处理方法包括添加同位素内标吡虫啉²D4,乙腈提取,再用活性碳和Oasis(HLB)固相小柱净化。该方法采用正离子方式,多反应监测每种烟碱类杀虫剂各两对离子进行定性、定量分析。方法在0.01~0.4 mg/kg范围内具有良好的线性关系。实验了3个添加水平0.02、0.04和0.2 mg/kg,回收率范围为80.1%~106.1%;相对标准偏差小于9.7%;方法检出限(LOQ)均为0.02 mg/kg。本方法简便、快速、准确,各项技术指标满足国内外法规的要求,可用于茶叶样品中烟碱类农药残留的确证检测。
【关键词】 茶叶
液相色谱 电喷雾电离三级四极杆质谱法 烟碱 农药残留
1 引言烟碱类杀虫剂是20世纪70年代壳牌公司发明的一类新化合物, 这类化合物作用于烟碱样乙酰胆碱受体(nicotin acetylcholine receptors, nAChRS),且结构中含有硝基亚甲基杂环的四氢²1,3²噻嗪(nithiazine,SKI²71),称为第一代烟碱类杀虫剂。为了改进其不稳定性而引入含氮原子的芳杂环甲基基团作为2²硝基亚甲基咪唑烷五元环系统的氯代烟碱类称为第二代烟碱类杀虫剂。迄今为止,已有以吡虫啉为代表的十几种新烟碱类杀虫剂产品相继商品化,如: 吡虫啉(imidacloprid)、啶虫脒(acetamiprid)、噻虫嗪(thiamethoxam)、噻虫啉(thiacloprid)、噻虫胺(clothiandin)及呋虫胺(dinotefur)。也有文献认为呋虫胺只有3²四氢呋喃甲基结构,而不具有其它新烟碱类化合物所具有的吡啶结构,而把它称为第三代烟碱类杀虫剂[1,2]。烟碱类杀虫剂通过与烟碱型的乙酰胆碱受体结合,使昆虫异常兴奋,全身痉挛麻痹而死,对粮食作物、油料、蔬菜及水果等多种虫害有防治效果。吡虫啉近年在我国茶叶生产中应用较广,用以防治小绿叶蝉、黑刺粉虱,能替代噻嗪酮。日本规定茶叶中6种烟碱类农药最高残留限量(MRLs)为10~50 mg/kg[3]; 欧盟规定茶叶中吡虫啉、啶虫咪的MRLs分别为0.05和0.1 mg/kg。
目前文献报道用高效
液相色谱法测定(HPLC)测定茶叶、蔬菜、水果中吡虫啉[4~6]的残留。上述方法检出限在0.03~0.05 mg/ kg之间;随着LC²ESI²MS/MS技术发展的日趋成熟,该方法被广泛用于测定和确证食品中农药残留。文献[6~9]检测蔬菜、茶叶和水果中吡虫啉或啶虫脒,方法的检出限为0.001~0.05 mg/kg。文献[10]检测蜂蜜中啶虫脒、吡虫啉、噻虫嗪农药,方法的检出限为0.01~0.1 mg/kg。文献[11]检测桃子、梨、小胡瓜、芹菜和杏中啶虫脒、吡虫啉、噻虫啉、噻虫嗪方法检出限为0.1~0.5 mg/kg。茶叶较蔬菜、水果等样品杂质干扰大、色素深,样品净化难度大。目前尚未见检测茶叶中6种烟碱类杀虫剂的
液相色谱²质谱/质谱法的报道。本实验提出了添加同位素内标吡虫啉²D4,用乙腈提取茶叶中6种烟碱类农药,再用活性碳和Oasis(HLB)固相小柱净化,LC²ESI²MS/MS测定。
2 实验部分
2.1 仪器与试剂
API4000
液相色谱²串联质谱仪:配有电喷雾离子源和大气压化学源(美国AB公司);活性碳SPE柱(500 mg, 6cc, Supecol公司);Oasis HLB SPE柱(500 mg, 6cc, Waters公司)。
甲醇、乙腈为色谱纯;无水Na2SO4为分析纯;呋虫胺、噻虫嗪、噻虫胺、吡虫啉、啶虫咪、噻虫啉和吡虫啉²D4标准物质(纯度≥97.5%,Dr Ehrenstorfer GmbH公司);储备液用甲醇配制,贮存在4 ℃的冰箱中,根据需要用乙腈²0.15%甲酸溶液(3∶7,V/V)溶液稀释至适当浓度的标准工作液。实验用水为Milli²Q高纯水。
2.2
液相色谱与质谱条件
ZORBAX Eclipse XDB²C8色谱柱(150 mm×4.6 mm, 5 μm);流动相:乙腈(A)和0.15%甲酸溶液(B), 梯度洗脱程序: 0 min时,30% A; 0~3.5 min,线性增加至70% A;8~10 min,降至30% A,之后进行系统平衡。流速:0.4 mL/min;进样量:20 μL。
扫描方式:正离子扫描;检测方式:多反应监测;电喷雾电压:4800 V;雾化气压力(GS1): 0.289 MPa;气帘气压力: 0.172 MPa;辅助气压力(GS2): 0.31 MPa;离子源温度: 540 ℃;碰撞气:0.0414 MPa;
2.3 样品处理
称取0.500 g茶叶样品置于50 mL塑料离心管中,加1 mL水浸泡0.5 h, 加入0.4 mL吡虫啉²D4(100 μg/L)和10 mL乙腈,均质,离心,将上层乙腈提取液过无水Na2SO4柱置于浓缩瓶,以除去乙腈中的少量水,再加入10 mL乙腈,重复上述操作,合并乙腈提取液,再用5 mL乙腈洗涤无水Na2SO4柱,在低于50 ℃的水浴中减压浓缩至约4 mL,待过柱。上述溶液转移至活性碳小柱(用5 mL乙腈预洗),再用5 mL乙腈洗脱,收集全部洗脱液,在低于50 ℃的水浴中减压浓缩至近干。用10 mL水分两次将残渣转移至Oasis HLB 小柱中(依次用5 mL甲醇,5 mL水预洗),再用5 mL水和5 mL V(甲醇)∶V(水)=1∶9的混合溶液依次洗涤浓缩瓶,洗涤液过固相萃取小柱,弃去流出液,在负压下抽干。用6 mL甲醇洗脱,控制流速在1~2 mL/min,收集全部洗脱液于10 mL离心管中。洗脱液在低于50 ℃的水浴中减压浓缩至近干,用2.0 mL V(乙腈)∶V(0.15%甲酸)=3∶7的混合溶液溶解,过0.45 μm滤膜,滤液待测。