维权声明:本文为v2778238原创作品,本作者与仪器信息网是该作品合法使用者,该作品暂不对外授权转载。其他任何网站、组织、单位或个人等将该作品在本站以外的任何媒体任何形式出现均属侵权违法行为,我们将追究法律责任。
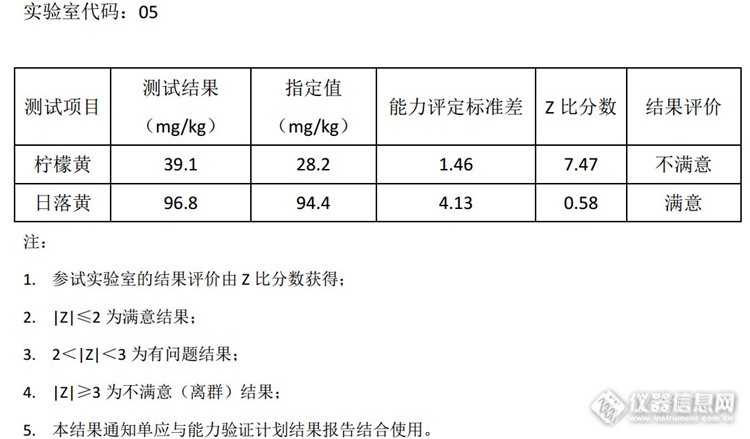
七月初参加了仪器信息网举办的饮料中柠檬黄日落黄的草根比对,8月初我们收到了举办方反馈回来的结果,如下
![]()
我们柠檬黄结果偏离了指定值很多。柠檬黄的结果为什么会出现这么大的偏离,是实验过程存在问题,还是数据处理问题? 我们初步怀疑是采用的254nm紫外光区检测波长存在干扰,因此再次向举办方申请样品,通过实验来查找问题所在。
由于本次实验是与检科院的能力实验样品一起做,检科院的样品过于稠厚,无法固相萃取,所以我们做了一些改变
1根据国标采用了聚酰胺粉吸附净化洗脱
2洗脱液由乙醇-氨水-水改成氨水-甲醇溶液
3检测波长除254nm外,增加检测波长430nm,480nm
实验准备
前处理用: 20%柠檬酸溶,实测PH=1.38
甲酸-甲醇液(体积比4+6)
氨水-甲醇(2%):(200ml容量瓶放4ml浓氨水加甲醇定容至刻度),
PH=4水:100ml纯水加2滴20%的柠檬酸液,实测PH=3.30
PH=6水:直接用纯水,实测PH=6.02
聚酰胺粉,G3垂融漏斗
流动相:
甲醇:Amethyst Chemicals HPLC/ACS
乙酸铵溶液:0.02mol/L,0.45μm滤膜抽滤后使用
标准品 中国计量科学研究院购买食用合成色素柠檬黄溶液标准物质(编号GBW(E)100001a),浓度为0.500 mg/mL,食用合成色素日落黄溶液标准物质(编号 GBW(E)100003a),浓度为0.500mg/mL
标系配制 1预实验配制20ug/mL的标准点进样,取样品过0.45μm滤头直接进样,粗略估计样品中目标组分含量范围,确定标准曲线的范围
2取10mL比色管5个,加入柠檬黄标准溶液各0.1,0.2, 0.4 ,0.,6, 0.8mL纯水定容至10mL,
标准系列溶液 柠檬黄(μg/mL)5 10 20 30 40
仪器与设备 戴安
液相色谱(P680 HPLC) UVD170U紫外检测器
VIS-1: 254nm VIS-2 : 430nm VIS-3: 480nm
色谱柱:安捷伦柱 5μm 4.6*250mm
样品前处理 1
. 根据样品中色素含量的高低,在千分之一电子天平上称样5-10g于50ml玻璃离心管,记录重量,然后称重1g聚酰胺粉用5ml水混匀后加入样品管,再用5ml水洗涤后一并加入,定容到25ml,每个样品管涡旋2min,静置1小时以上,再涡旋2min(如时间紧,可涡旋一次)
![]()
2
.将离心管中样品振摇混匀后,倾入G3垂融漏斗,尽量搅匀,使固形物均匀下沉形成厚度一致的聚酰胺层,便于除杂洗脱
![]()
3. 聚酰胺混合液在垂融漏斗中静置沉降一会后,真空抽走液体,进入洗涤程序
A:用pH=4的水,每次10ml洗涤2次,5ml洗涤1次,可真空抽提
B:用甲醇-甲酸溶液,每次10ml洗涤2次,5ml洗涤1次,可真空抽提
C:用纯水洗涤,至流出液呈中性,每次10ml洗涤3次以上,可真空抽提
4. 解吸 用2%的氨水甲醇液解吸,首次加入7ml解吸液,不要抽提,通过重力自然洗脱,收集于10ml比色管,尽量使聚酰胺层洗至无色,置氮吹仪吹净甲醇和氨,近干,加纯水定容至10ml待测
液相色谱分析(进样20μL)
1 标准曲线回归方程 | | 254nm | 430nm | 480nm |
柠
檬
黄 | ŷ=14.842x+5.420 | ŷ=15.208x+5.929 | ŷ=3.681x+2.255 |
r=0.9998 | r=0.9998 | r=0.9999 |
2样品分析 | | 柠檬黄 |
直接进样 | 聚酰胺粉净化 |
254nm | 峰高 | 534.72 | 536.05 | 221.52 | 221.65 |
| 结果(mg/kg) | 70.16 | 28.62 |
430nm | 峰高 | 244.91 | 243.76 | 227.38 | 227.51 |
| 结果(mg/kg) | 30.80 | 28.62 |
480nm | 峰高 | 61.03 | 61.05 | 55.63 | 55.68 |
| 结果(mg/kg) | 31.38 | 28.50 |
从数据可以看出,直接进样检测,结果是偏高的,特别是254nm处,聚酰胺粉净化后进样结果都在可接受范围
注:样品指定值 柠檬黄
(mg/kg):28.3±1.41
回收率
| | | 柠檬黄 |
| | | 样品 | 样品加标(10ug/ml) |
254nm | 峰高 | 197.28 | 197.58 | 344.36 | 343.36 |
浓度(ug/mL) | 12.93 | 12.95 | 22.84 | 22.77 |
均值(ug/mL) | 12.94 | 22.805 |
回收率(%) | 98.6 |
430nm | 峰高 | 202.56 | 202.78 | 353.61 | 352.36 |
浓度(ug/mL) | 12.93 | 12.94 | 22.86 | 22.78 |
均值(ug/mL) | 12.935 | 22.82 |
回收率(%) | 98.8 |
480nm | 峰高 | 49.49 | 49.73 | 85.83 | 85.64 |
浓度(ug/mL) | 12.83 | 12.90 | 22.70 | 22.65 |
均值(ug/mL) | 12.865 | 22.675 |
回收率(%) | 98.1 |
结果分析 从结果来看,采用聚酰胺粉直接净化,柠檬黄在三个波长检测的结果一致,254nm波长处并未出现我们最初怀疑的紫外区的吸收干扰,这使我们感到困惑,第一次出现的结果偏高的原因在哪?
由于此次实验和上次相比,我们改变了一些条件,为了重现上次的实验过程,我们又重新采用6ml固相萃取柱作前处理,并分别采用两种解吸液解吸,验证不同的解吸液对实验结果的影响。
结果见下表
| | | 柠檬黄 | 日落黄 |
乙醇-氨水-水 | 氨水-甲醇 | 乙醇-氨水-水 | 氨水-甲醇 |
254nm | 结果(mg/kg) | 37.2 | 39.0 | 93.9 | 96.0 |
430nm | 结果(mg/kg) | 27.9 | 29.2 | 93.9 | 96.1 |
480nm | 结果(mg/kg) | 28.3 | 29.5 | 95.1 | 97.3 |
对比实验数据发现采用固相萃取柱净化,柠檬黄在254nm处的检测结果明显偏高同时实验结果显示,两种解吸液在固相萃取柱上解吸,氨水-甲醇液解吸液的结果略高于乙醇-氨水-水的萃取结果,由于数据偏少,这个结论有待于更多的实验确认。
所有数据汇总如下表 | 柠檬黄 |
| | 聚酰胺粉净化 | 固相萃取柱萃取 |
| 254nm | 峰高 | 221.52 | 221.65 | 274.27 | 275.36 |
浓度(ug/mL) | 14.56 | 14.57 | 18.97 | 19.05 |
结果(mg/kg) | 28.6 | 28.6 | 37.12 | 37.28 |
| 430nm | 峰高 | 227.38 | 227.51 | 221.87 | 224.01 |
浓度(ug/mL) | 14.56 | 14.57 | 14.83 | 14.98 |
结果(mg/kg) | 28.6 | 28.6 | 29.0 | 29.3 |
| 480nm | 峰高 | 55.63 | 55.68 | 54.55 | 55.10 |
浓度(ug/mL) | 14.50 | 14.51 | 15.00 | 15.17 |
结果(mg/kg) | 28.5 | 28.5 | 29.4 | 29.7 |
由此可以看出我们在七月初参加的饮料中草根对比试验中,采用固相萃取柱净化,并以254nm作为检测波长,色素柠檬黄检测结果确实会偏高。这种现象是这一品牌固相萃取柱特有的现象还是共同的现象,我们又对比做了另外一品牌固相萃取柱,结果如下:
| | | 柠檬黄 |
| 固相萃取柱(品牌A) | 固相萃取柱(品牌B) |
254nm | 结果(mg/kg) | 37.12 | 37.28 | 38.59 | 38.43 |
430nm | 结果(mg/kg) | 29.02 | 29.32 | 28.85 | 28.85 |
480nm | 结果(mg/kg) | 29.35 | 29.69 | 29.14 | 29.12 |
从数据可以看出,采用固相萃取柱净化,柠檬黄在254nm处的检测结果会明显偏高,对此我们怀疑是不是固相萃取柱本身会带入在紫外区254nm处有吸收的物质影响检测结果,于是加做了全程含固相萃取柱净化流程的空白实验,品牌A和品牌B固相萃取后空白液254nm吸收谱图如下:
![]()
由上述谱图看出两种固相萃取柱空白解吸液在254nm处柠檬黄吸收值为零,也就是固相萃取柱本身并未带入254nm处有吸收的成分,那么样品中柠檬黄采用固相萃取净化,选择254nm测试结果偏高的到底是什么原因?此次实验仍未找到结论,只是发现样品中色素柠檬黄采用固相萃取净化,在254nm处检测存在很大风险
综上所述,针对样品中色素柠檬黄的检测,:一是可采用聚酰胺粉直接净化,二是采用430nm或480nm波长作测试波长。