维权声明:本文为v3127170原创作品,本作者与仪器信息网是该作品合法使用者,该作品暂不对外授权转载。其他任何网站、组织、单位或个人等将该作品在本站以外的任何媒体任何形式出现均属侵权违法行为,我们将追究法律责任。
离子色谱法同时测定药品中巴比妥酸和5种无机阴离子的研究
黄选忠
(湖北兴山县疾病预防控制中心,湖北兴山,443700)
摘要
建立离子色谱-抑制电导检测法同时测定巴比妥酸和F
-、Cl
-、NO
3-、H
2PO
4-和SO
42-等5种无机阴离子的新方法。以SH-AP-2型阴离子交换柱为分离柱,以6.0mmol/LNa2CO3-1.0mmol/LNaHCO
3溶液为淋洗液,流量为0.80 mL/min,采用等度洗脱的方式可将巴比妥酸与F
-、Cl
-、NO
3-、H
2PO
4-和SO
42-等5种常见无机阴离子完全分离,巴比妥酸和SO
42-,NO
3-、Cl
-和H
2PO
4-,F
-的峰面积与其质量浓度分别在0.10~20.0mg/L、0.05~10.0mg/L和0.04~8.0mg/L范围内呈良好的线性关系,相关系数r在0.9994~0.9999,方法应用于巴比妥、苯巴比妥和维生素B12等药品中巴比妥酸和F
-、Cl
-、NO
3-、H
2PO
4-和SO
42-等无机阴离子的同时测定,加标回收率在92.6%~104.0%,5次平行测定结果的相对标准偏差(RSD)在1.06%~3.89%,最低检出限在0.01mg/L~0.06mg/L,方法回收率较高、重现性良好,操作简便快速,可用于巴比妥、苯巴比妥和维生素B12等样品中巴比妥酸和F
-、Cl
-、NO
3-、H
2PO
4-和SO
42-等
无机阴离子的定量分析。关键词
离子色谱法;
巴比妥酸;
无机阴离子;巴比妥;苯巴比妥;维生素B12中图分类号:O652.63 文献标识码: 文章编号:
Ion chromatography for the simultaneous determination of barbituric acid
and five inorganic anions in pharmaceutical products
HUANG Xuanzhong
(Prevention and Health Protection Centre of Hubei Xingshan County,HubeiXingshan 443700, China)
A new method for the simultaneous determination of barbituric acid and F
-, Cl
-, NO
3-, H
2PO
4- and SO
42- by ion chromatography-suppressed conductivity detection was established. With SH-AP-2 anion exchange column as the separation column and 6.0mmol/LNa
2CO
3-1.0mmol/LNaHCO
3 solution as the eluent, the flow rate was 0.80 mL/min, barbituric acid and five common inorganic anions such as F
-, Cl
-, NO
3-, H
2PO
4- and SO
42- were completely separated by isocratic elution, The peak area of barbituric acid and SO
42- , NO
3-, Cl
- and H
2PO
4-, F
- showed a good linear relationship with their mass concentrations in the range of 0.10
~20.0mg/L, 0.05
~10.0mg/L and 0.04
~8.0mg/L , and the correlation coefficient r was 0.9994
~0.9999, respectively.The method was applied to the simultaneous determination of barbituric acid and inorganic anions such as F
-, Cl
-, NO
3-, H
2PO
4- and SO
42- in barbiturates, phenobarbital and vitaminB
12 drugs, with a recovery rate of 92.6%
~104.0%, a relative standard deviation (RSD) of 5 parallel measurement results of 1.06%
~3.89%, and the minimum detection limit was 0.01mg/L
~0.06mg/L. It can be used for the quantitative analysis of barbituric acid and inorganic anions such as F
-, Cl
-, NO
3-, H
2PO
4- and SO
42- in samples such as barbiturates, phenobarbital and vitaminB
12.
Key words
ion chromatography;barbituric acid;Inorganic anions;barbiturates;phenobarbital;vitaminB12 巴比妥酸(BA)是合成巴比妥、苯巴比妥等镇静催眠药和维生素B12等药品的中间体[1],在这些合成药品中可能残留有微量的BA而影响品质,F-、NO3-、H2PO4-等无机阴离子过量摄入会影响人体健康,因此监测巴比妥、苯巴比妥和维生素B12等药品中微量BA和F-、NO3-、H2PO4-等无机阴离子含量对保障用药安全具有重要意义。目前测定药品中微量BA的方法已报道的有化学发光法[2]和分光光度法[3],其中,化学发光法需要专用仪器,而分光光度法则灵敏度偏低。离子色谱法目前已成为测定无机阴离子的常用方法,已广泛应用于药品中无机阴离子的同时测定[4-10]。本实验研究用SH-AP-2型阴离子交换柱和CIC-100型色谱仪同时测定巴比妥等药品中的BA和F-、Cl-、NO3-、H2PO4-和SO42-等5种无机阴离子的色谱条件和可行性,结果表明,以SH-AP-2型阴离子交换柱为分离柱、6.0mmol/LNa2CO3-1.0mmol/LNaHCO3溶液为淋洗液,流量为0.80ml/min,采用等度洗脱的方式可使BA和F-、Cl-、NO3-、H2PO4-和SO42-等5种无机阴离子完全分离,且BA和SO42-,NO3-、Cl-和H2PO4-,F-的峰面积与其质量浓度分别在0.10~20.0mg/L、0.05~10.0mg/L和0.04~8.0mg/L范围内呈良好的线性关系,相关系数r≥0.9994,方法应用于巴比妥、苯巴比妥和维生素B12等样品中F-、Cl-、NO3-、BA、H2PO4-和SO42-的同时测定, 加标回收率分别为99.2%~100.9%、101.0%~103.8%、96.1%~103.0%、92.6%~104.0%、94.6%~101.9%和98.6%~101.0%,5次平行测定结果的RSD分别为1.23%~2.38%、1.15%~1.89%、1.06%~2.11%、1.11%~3.89%、2.05%~3.66%和1.09%~3.05%,按3倍信噪比(3N/b)计,最低检出限在0.01mg/L~0.06mg/L,方法适用于巴比妥、苯巴比妥和维生素B12等样品中F-、Cl-、NO3-、BA、H2PO4-和SO42-的同时测定。1 实验部分
1.1 主要仪器与试剂离子色谱仪:CIC-100,青岛盛瀚色谱公司。抑制器:SHY-2型自再生抑制器,青岛盛瀚色谱公司。
定量环体积:25μL;自动进样器:SHA—15型,青岛盛瀚色谱公司。0.45μm滤膜过滤器:13 mm,青岛盛瀚色谱公司。
巴比妥酸(C
4H
4N
2O
3·2H
2O):分析纯((含量
≥98.5%)),国药集团化学试剂有限公司。
BA标准溶液:1000mg/L,称取0.1301g巴比妥酸,溶解于高纯水,定容至100ml容量瓶。
磷酸二氢钾、溴化钾:分析纯,国药集团化学试剂有限公司。
H
2PO
4-和Br
-标准溶液:1000 mg/L,按照文献[11]配制。
NO
3-、F
-、Cl
-、SO
42-标准溶液:
质量浓度均为1000 mg/L,编号分别为GBW(E)080264、GBW(E)080549、GBW(E)080268、GBW(E)080266;NO
2-标准溶液:
质量浓度为100 mg/L,编号为GBW(E)080223,北京中国计量科学研究院。
无水碳酸钠、碳酸氢钠:分析纯,国药集团化学试剂有限公司。
实验所用其它试剂均为AR级。
实验用水为高纯水(电阻率为18.2ΜΩ·cm)。
1.2 仪器工作条件色谱分离柱:SH-AP-2型阴离子交换柱(250×4.0mm i.d,青岛盛瀚色谱公司,批号:2004005);保护柱:SH-AP-2型保护柱(50×4.0mm i.d,青岛盛瀚色谱公司,批号:G200023)。
淋洗液:6.0mmol/LNa2CO3-1.0mmol/LNaHCO
3溶液,流量为0.80ml/min;柱箱温度:35℃;电流:75mA;检测器:电导检测器;自动进样器:全定量环取样,取样后清洗(每针之间),置换量70μL,取样量25μL,扎针深度4mm。
1.3 实验方法
1.3.1 标准溶液配制 BA和F
-、Cl
-、NO
3-、H
2PO
4-和SO
42-混合标准
应用液:临用前将各种标准溶液逐级稀释成含5.0mg/L的BA和SO
42-、2.50mg/L的Cl
-、NO
3-、H
2PO
4-和2.0mg/L的F
-(A液)和50.0mg/L的BA和SO
42-、25.0mg/L的Cl
-、NO
3-、H
2PO
4-和20.0mg/L的F
-(B液)标准应用液。
取上述混合标准
应用液A液0.20、1.00mL及B液0.20、0.40、1.0、2.0、4.0mL于7只10mL容量瓶中加纯水至刻度,混匀,配制成含BA和SO
42-均为
0.10、0.50、1.00、2.00、5.00、10.00、20.00mg/L,含Cl
-、NO
3-、H
2PO
4-均为
0.05、0.25、0.50、1.00、2.50、5.00、10.00mg/L和含F
-为0.04
、0.20、0.40、0.80、2.00、4.00、8.00mg/L的系列标准工作溶液。1.3.2标准曲线绘制 取1.3.1制备的系列标准工作溶液,各管1.5mL于样品瓶中,启动自动进样器进样,分别测定各组分的峰面积,以各组分的峰面积(y)为纵坐标,以色谱峰面积对应的组分质量浓度(x)为横坐标,绘制工作曲线。
1.3.3 样品处理
称取巴比妥0.250g加5
mL无水乙醇溶解后,用高纯水定容至100ml,取该样液
用高纯水稀释1倍并经0.45μm滤膜过滤后供测试,样品测试液中巴比妥的质量浓度为1250
mg/L。取苯巴比妥片(30
mg苯巴比妥/片)5片研碎加10
mL无水乙醇充分研磨溶解后,用高纯水定容至100ml,滤去不溶物,滤液
用高纯水稀释1倍并经0.45μm滤膜过滤后供测试,样品测试液中苯巴比妥的质量浓度为750
mg/L。取维生素B
12片40片(含维生素B
12约1000
μg)用
高纯水洗去表面糖衣后,加高纯水充分研磨溶解并
定容至100ml,滤去不溶物,滤液
用0.45μm滤膜过滤后供测试,样品测试液中维生素B
12的质量浓度为10
mg/L。1.3.4样品测定
取1.3.3的样品测试液1.5ml于样品瓶中,启动自动进样器进样测定各组分的峰面积,以标准曲线法定量,同时进行加标回收试验。
2 结果与讨论
2.1 色谱条件的选择
2.1.1 淋洗液的选择
试验分别以5.0mmol/L、6.0mmol/L、8.0mmol/L和10.0mmol/LNa
2CO
3溶液为淋洗液,考察了SH-AP-2型柱对BA和F
-、Cl
-、NO
3-、H
2PO
4-和SO
42-等常见阴离子的分离情况,结果表明,当Na
2CO
3溶液超过6.0mmol/L时,H
2PO
4-和SO
42-二者合并为一个峰,这与文献
[12]报道的情况相似,因此要将前述6种组分完全分离,不宜以单纯Na
2CO
3溶液为淋洗液,应以Na
2CO
3/NaHCO
3混合溶液为淋洗液, Na
2CO
3与NaHCO
3溶液浓度配比试验结果见表1,从表1可见,随着淋洗液中NaHCO
3浓度的增加,NO
3-的峰分离度(R)逐渐降低,BA的峰分离度则无明显的改变,而F
-、Cl
-和H
2PO
4-的峰分离度逐渐增加,为使NO
3-与H
2PO
4-均有适宜的峰分离度,本试验以
6.0mmol/LNa2CO3-1.0mmol/LNaHCO
3溶液为淋洗液,在此淋洗条件下F
-、Cl
-、NO
3-、BA、H
2PO
4-和SO
42-的分离色谱图见图1。
表1 Na2CO3与NaHCO3不同配比对各组分峰分离度(R)的影响(流量0.80 ml/min,柱箱温度35℃)
组分 | Na2CO3+NaHCO3(mmol/L) |
6.0+0 | 6.0+0.9 | 6.0+1.0 | 6.0+1.1 | 6.0+2 | 6.0+3.0 |
F- | 2.90 | 3.05 | 3.06 | 3.07 | 3.15 | 3.36 |
Cl- | 5.74 | 6.05 | 6.06 | 6.07 | 6.45 | 6.63 |
NO3- | 2.02 | 1.61 | 1.53 | 1.54 | 1.27 | 1.08 |
BA | 3.97 | 3.75 | 3.57 | 3.48 | 3.55 | 3.16 |
H2PO4 | 二者合并为一个峰 | 1.47 | 1.63 | 1.62 | 2.27 | 2.88 |
SO42- | / | / | / | / | / |
2.1.2 淋洗液流量的影响
考察了淋洗液流量分别为0.70、0.80和0.90 mL/min时各组分的分离情况,试验结果见表2,从表2![]()
图1 F-、Cl-、NO3-、BA、H2PO4-和SO42-分离效果图
可见,随着淋洗液流量的升高,各组分
的保留时间(T)逐渐缩短,峰分离度(R)逐渐减小(NO
3-和H
2PO
4-除外),
表2 淋洗液流量的影响(6.0mmol/LNa2CO3-1.0mmol/LNaHCO3溶液,柱箱温度35℃)
组分 | 0.70ml/min | 0.80ml/min | 0.90ml/min |
T/min | R | 峰面积 | T/min | R | 峰面积 | T/min | R | 峰面积 |
F- | 5.955 | 3.19 | 836046 | 5.212 | 3.08 | 735031 | 4.666 | 3.02 | 672656 |
Cl- | 8.155 | 6.33 | 883680 | 7.137 | 6.14 | 775756 | 6.397 | 6.05 | 695800 |
NO3- | 12.156 | 1.43 | 940957 | 10.633 | 1.52 | 854040 | 9.536 | 1.38 | 730092 |
BA | 13.299 | 3.60 | 521413 | 11.657 | 3.55 | 456506 | 10.440 | 3.53 | 403955 |
H2PO4 | 16.672 | 1.89 | 385185 | 14.578 | 1.67 | 311122 | 13.066 | 1.83 | 300895 |
SO42- | 18.392 | / | 1314478 | 16.036 | / | 1151063 | 14.388 | / | 1016420 |
峰面积逐渐降低,
为使组分有较短的保留时间、较高的峰分离度(≧1.5)和检测灵敏度、
系统有较低的压力,综合考虑,本试验确定的淋洗液流量为0.80mL/min。2.1.3 柱箱温度的选择
考察了柱箱温度为30℃、35℃、40℃时各组分的分离效果,结果见表3,从表3可见,随着柱温的升高,Cl
-、NO
3-和BA的
T稍微缩短,而F
-、H
2PO
4-和SO
42-的T则稍微延长,各组分
峰面积逐渐增加(BA除外),BA和H
2PO
4-的
R逐渐增加,而F
-、Cl
-先降后增,NO
3-则反之
,综合考虑待测组分的检测灵敏度和峰分离度,本试验选择的柱箱温度为35℃。
表3 柱箱温度选择试验结果(6.0mmol/LNa2CO3-1.0mmol/LNaHCO3溶液,流量0.80 ml/min)
组分 | 30℃ | 35℃ | 40℃ |
T/min | R | 峰面积 | T/min | R | 峰面积 | T/min | R | 峰面积 |
F- | 5.207 | 3.02 | 739319 | 5.218 | 2.88 | 794144 | 5.239 | 2.96 | 863877 |
Cl- | 7.184 | 5.97 | 730106 | 7.162 | 5.79 | 754818 | 7.087 | 5.82 | 850656 |
NO3- | 10.757 | 1.47 | 816408 | 10.611 | 1.51 | 841047 | 10.426 | 1.48 | 904089 |
BA | 11.905 | 3.00 | 451962 | 11.705 | 3.40 | 452106 | 11.416 | 3.84 | 440461 |
H2PO4 | 14.447 | 1.43 | 273433 | 14.537 | 1.64 | 318123 | 14.586 | 1.85 | 367593 |
SO42- | 15.517 | / | 1018577 | 15.793 | / | 1142753 | 16.108 | / | 1237767 |
2.2
共存物质的影响 分别取1.1所列各种标准溶液配制成含12mg/L的BA、4mg/L的NO
3-、H
2PO
4-和SO
42-、1
mg/L的F
-、2
mg/L的Cl
-、5mg/L的NO
2-和Br
-的混合标准溶液,以考察NO
2-和Br
-与6种待测
组分的分离效果,见图2,从图2可知,在本试验条件下,NO
2-和Br
-与硝6种待测
组分可以完全分离,均不影响
F
-、Cl
-、NO
3-、BA、H
2PO
4-和SO
42-等组分的测定。
![]()
图2 BA与常见阴离子色谱图
2.3 线性方程、线性范围与检出限按照1.3.1配制标准系列,测定 F
-、Cl
-、NO
3-、BA、H
2PO
4-和SO
42-等组分的峰面积,以峰面积(y)为纵坐标,以其质量浓度(x)为横坐标绘制标准曲线,进行线性回归。测定仪器30min的基线噪声,以3倍基线噪声除以标准曲线的斜率(3N/b)计算各组分的最低检出限。其标准曲线的线性范围、回归方程、相关系数r(回归方程的截距、斜率和r均由仪器软件自动生成)、检出限列于表4。从表4可见,
BA和SO
42-,NO
3-、Cl
-和H
2PO
4-,F
-的峰面积与其质量浓度分别在0.10~20.0mg/L、0.05~10.0mg/L和0.04~8.0mg/L范围内呈良好的线性关系,相关系数r在0.9994
~0.9999,检出限分别为0.01mg/L
~0.06mg/L。其中,2.0mg/L的
BA和SO
42-、1.0mg/L的NO
3-、Cl
-和H
2PO
4-和0.80mg/L的F
-的标准色谱图见图3。
表4 BA等6种组分的线性范围、回归方程、相关系数和检出限
组分 | 线性范围/mg/L | 回归方程 | 相关系数/r | 检出限/mg/L |
F- | 0.04~0.80 | S=608900C+172700 | 0.9999 | 0.01 |
Cl- | 0.05~10.0 | S=369700C-7110 | 0.9999 | 0.01 |
NO3- | 0.05~10.0 | S=101100C+2467 | 0.9999 | 0.02 |
BA | 0.10~20.0 | S=34990C-2426 | 0.9999 | 0.06 |
H2PO4- | 0.05~10.0 | S=83140C-2426 | 0.9994 | 0.03 |
SO42- | 0.10~20.0 | S=270800C-9792 | 0.9998 | 0.01 |
![]()
图3 F-、Cl-、NO3-、BA、H2PO4-和SO42-的标准色谱图
2.4 样品测定及加标回收试验按1.3.3和1.3.4的步骤操作,测定巴比妥、苯巴比妥和维生素B
12等样品中的
F
-、Cl
-、NO
3-、BA、H
2PO
4-和SO
42-的含量。并在3种样中分别添加混合标准应用液(B液)0.20、0.40和2.00
mL配制成加标样品,各平行测定5次,计算加标回收率及测定结果的相对标准偏差(RSD),结果见表5。由表5可知,
F
-、Cl
-、NO
3-、BA、H
2PO
4-和SO
42-的加标回收率分别为99.2%~100.9%、101.0%~103.8%、96.1%~103.0%、92.6%~104.0%、94.6%~101.9%和98.6%~101.0%,5次平行测定结果的RSD分别为1.23%~2.38%、1.15%~1.89%、1.06%~2.11%、1.11%~3.89%、2.05%~3.66%和1.09%~3.05%,方法的回收率较高、重现性良好,巴比妥、苯巴比妥和维生素B
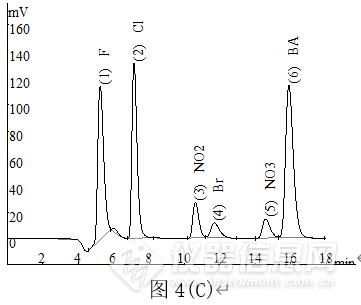
12加标样品色谱图见图4。
![]()
![]()
![]()
图4 巴比妥(A)、苯巴比妥(B)和维生素B12(C)加标样品色谱图
表5 巴比妥、苯巴比妥和维生素B12样品测定及加标回收试验结果
组分 | 巴比妥(1250mg/L) | 苯巴比妥(750mg/L) | 维生素B12(10mg/L) |
本底/mg/L | 加入量/mg/L | 回收率/% | RSD/% | 本底/mg/L | 加入量/mg/L | 回收率/% | RSD/% | 本底/mg/L | 加入量/mg/L | 回收率/% | RSD/% |
|
F- | <0.01 | 0.40 | 100.9 | 2.38 | 0.091 | 0.80 | 99.2 | 1.23 | <0.01 | 4.00 | 99.5 | 1.26 |
Cl- | 0.138 | 0.50 | 101.0 | 1.15 | 2.37 | 1.00 | 103.8 | 1.89 | 2.23 | 5.00 | 101.5 | 1.55 |
NO3- | 0.024 | 0.50 | 103.0 | 2.11 | 0.521 | 1.00 | 96.1 | 1.68 | 1.08 | 5.00 | 100.6 | 1.06 |
BA | <0.06 | 1.00 | 92.6 | 1.11 | <0.06 | 2.00 | 94.1 | 3.89 | <0.06 | 10.00 | 104.0 | 2.27 |
H2PO4- | <0.03 | 0.50 | 101.9 | 2.37 | <0.03 | 1.00 | 94.6 | 3.66 | 0.182 | 5.00 | 98.3 | 2.05 |
SO42- | 0.258 | 1.00 | 101.0 | 2.52 | 0.626 | 2.00 | 98.6 | 2.30 | 3.15 | 10.00 | 100.8 | 1.09 |
3 结语
建立了
以SH-AP-2型阴离子交换柱为分离柱,以6.0mmol/LNa2CO3-1.0mmol/LNaHCO
3溶液为淋洗液,流量为0.80 mL/min等度洗脱,
离子色谱-抑制电导检测法同时测定F
-、Cl
-、NO
3-、BA、H
2PO
4-和SO
42-的新方法。方法应用于巴比妥、苯巴比妥和维生素B
12等样品中F
-、Cl
-、NO
3-、BA、H
2PO
4-和SO
42-同时的测定,加标回收率在92.6%~104.0%,5次平行测定结果的相对标准偏差(RSD)在1.06%~3.89%,最低检出限在0.01mg/L~0.06mg/L,方法回收率较高、重现性良好,操作简便快速,可用于巴比妥、苯巴比妥和维生素B
12等样品中BA等6种组分的定量分析。
参考文献
1)刘琪,梅洪波,刘野,等.镇静催眠药巴比妥酸的合成研究[J],辽宁化工,2019,48(1):33
2)罗挽兰,高华,何治柯,等.钌(Ⅱ)-联吡啶-巴比妥酸-Ce(Ⅳ)化学发光体系测定巴比妥酸的研究[J],分析科学学报,1996,12(2):142-144
3)黄选忠,郑林.巴比妥酸-NO
2--Fe(Ⅱ)-CPB显色体系光度测定巴比妥酸的研究[J],分析科学学报,1999,15(3):238-241
4)
谢玉惠,冉茂婷,龙兴浩.加速溶剂萃取-离子色谱法同时测定复方益母草颗粒中9种无机阴离子含量[J],中南药学,2016,14(8):854-8585)谢玉惠,龙兴浩.离子色谱法同时测定附子理中丸中9种无机阴离子[J],安徽医药,2016,20(8):1490-14936)王宇,黄勇.离子色谱法同时检测利咽灵片中9种无机阴离子[J],中药材,2017,40(10):2380-23827)周伟娥,杨立佼,谢巍,等.离子色谱法同时测定感冒清热颗粒中9种无机阴离子[J],中国药房,2015,26(18):2546-25498)蔡卓夫.离子色谱法定量测定硝酸异山梨酯片中硝酸盐的含量[J],中国药房,2014,25(1):78-799)胡恩泽,魏明,黄正辉.加速溶剂萃取-离子色谱法同时测定黄连上清片中9种常见无机阴离子的含量[J],中国药房,2017,28(12):1706-171010)陈柳生,蔡自由,周伟明.离子色普法测定维生素B
1注射液中的EDTA及硝酸根离子[J],中国实验方剂学杂志,2014,20(14):61-64
11)《水质分析大全》编写组. 水质分析大全[M]. 重庆:科学技术文献出版社重庆分社,1989:115-118
12)杜宏山,黄选忠,汪波,等.
离子色谱法同时测定环境水样中硫氰酸盐等8种阴离子的方法应用[J].预防医学情报杂志,2021,37(9):1290-1296