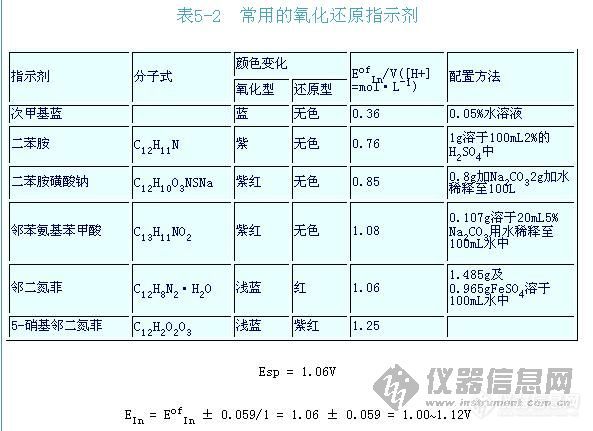
一、氧化还原指示剂
这类指示剂的氧化态和还原态具有不同的颜色,在滴定过程中指示剂由氧化态变为还原态,或由还原态变为氧化态。根据颜色的突变来指示终点。例如用K2Cr2O7溶液滴定Fe2+,常用二苯胺磺酸钠为指示剂,二苯胺磺酸钠的还原态为无色,氧化态为紫红色,故滴定到计量点后,过量一点K2Cr2O7就能使二苯胺磺酸钠由还原态转变为氧化态,溶液显紫红色,因而可以指示滴定终点。
如果用In(Ox)和In(Red)分别表示指示剂的氧化态和还原态,其氧化还原电对为
In(Ox) + ne = In(Red)
随着滴定过程中溶液电位值的变化,指示剂的[In(Ox)]/[In(Red)]变化
EIn = EofIn + 0.059/nlgCIn(Ox)/CIn(Red)
与酸碱指示剂的变色情况相似,当CIn(Ox)/CIn(Red)10时,溶液显氧化态的颜色,此时
EIn EofIn + 0.059/nlg10 = EofIn + 0.059/n
当CIn(Ox)/CIn(Red)1/10时,溶液呈还原态的颜色,此时
EIn EofIn + 0.059/nlg1/10 = EofIn-0.059/n
故指示剂的变色范围,EIn = EofIn ± 0.059/n(25οC)
在此范围的两侧可以看到指示剂颜色的改变,当被滴定溶液的电位值恰等于EofIn时,指示剂显中间颜色,一些常用的氧化还原指示剂列于表5-1。在实际滴定工作中,指示剂的变色范围应包括在滴定计量点前后0.1%的电位突跃范围内。例如在1.0mol·L-1H2SO4介质中,用Ce4+滴定Fe2+,前已计算出滴定计量点前后0.1%的电位突跃范围是0.86~1.26V,显然选择邻二氮菲亚铁作指示剂是合适的。
![]()
在突跃范围以内,若选用二苯胺磺酸钠为指示剂EIn=0.85±0.059/2=0.82~0.88V,与突跃范围只有很少一点重合,滴定误差必然很大,为了克服这个缺点,可在被滴定的溶液中加入一些H3PO4,它与Fe3+配位成稳定的[Fe(HPO4)]+,可以降低Fe3+/Fe2+电对的电位,使滴定突跃范围加大,计量点前按还原电对计算电位
E = EFe3+/Fe2+ + 0.059lgCFe3+/CFe2+
在计量点前99.9%的电位值为
E = EFe3+/Fe2+ + 0.059lg99.9/0.1
若使浓度降低10000倍
E=0.68+0.059lg=0.62V
即突跃范围电位变成0.62~1.26V,则二苯胺磺酸钠也是适宜的。
如前所述,氧化还原滴定反应的完全程度一般来说是比较高的,因而计量点附近的突跃范围较大,又有多种不同的指示剂可供选择,因此终点误差一般都不大,在此不作介绍。还必须指出,指示剂本身会消耗滴定剂。例如,二苯胺磺酸钠因氧化而由无色变为紫色时,需要消耗一定量的标准溶液,当标准溶液浓度比较大时,(例如0.1mol·L-1)氧化剂所消耗的标准溶液体积很小,对分析结果的影响不大。可以忽略不计,如果标准溶液的浓度很小。例如0.1mol·L-1时,就要作空白试验,测出指示剂所消耗的体积,作为空白值,然后从标准溶液的总体积中将空白值减去。