在两个 “电池” 中, 铜和碳棒是作为 “阴极” ,在其表面所发生的阴极反应,在一定
条件下并不是铜和碳棒本身(起导体作用) ,而是氧的作用。在左图的溶液中是溶解氧,
而在右图的“干电池”中是氧化剂。氧在阴极反应(还原反应)的表达式是:
2O2+H2O+4e=4OH -(2-2) ( Cu++ + 2e = Cu
如果左图溶液中有做足量 Cu++ ) (2H+ + 2e = H2 如果左图溶液是酸性的) 由上可以看出, 电化学过程至少需要以下四个基本条件:
(1) 要有阴极、阳极两个独立、分离的区域;
(2) 两极间存在、保持电位差;
(3) 两极间存在电子通路(导线) ;
(4) 两极间存在离子通路(液体、水等)
通常的化学反应,不需要以上条件,是物质间直接接触(碰撞)就可以发生的,这正是电化学反应不同于通常的化学反应之处。
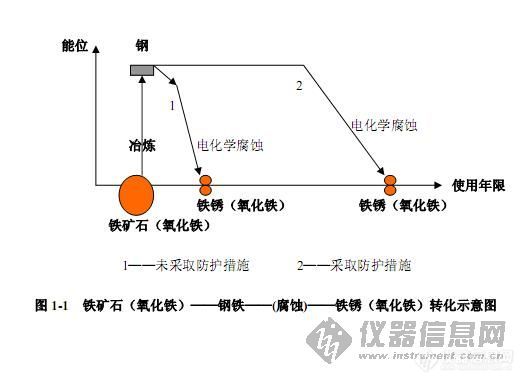
图 2-1 描述的铁、锌是处于阳极区,他们由原来的金属状态变成了离子状态,这种阳
极离解现象就是“腐蚀” 。它虽然发生在阳极, 但没有阴极和电子、 离子通路, 这个 “腐
蚀”是不能发生的。着正是电化学腐蚀的特点,也是钢铁和其他金属腐蚀的路径。
3. 平常只见到钢铁表面锈蚀,其中的“阴极” 、 “阳极”是怎样产生和区分的? 上面看到的是“大电池” (宏电池)腐蚀的形式,实际中,大量存在的是“微电池”腐蚀。 “微电池”与“大电池”在电化学原理上是一致的, “微电池”也必须满足上面提到的四个基本要素,只是“微电池”可能发生在极小的范围内(如金属晶粒之间) ,而一小快铁片上,可能存成千上万个“微电池” ,甚至宏观上难以区分阴极、阳极区。
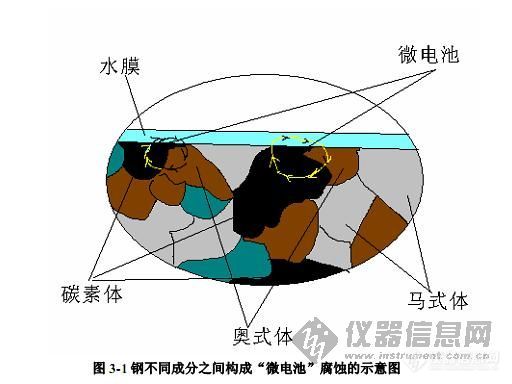
以下举例说明。我们知道,处在潮湿大气中的钢铁,表面很快会生锈。大多数情况下是“微电池”腐蚀的结果。图 3-1 描述了在显微镜放大的情况下所观察到的“微电池”腐蚀。我们知道钢的主要成分虽然是铁,但钢中还含有碳、磷、锰、硅等成分与杂质,同时形成碳素体、奥式体、马式体等不同的固溶体形式。当钢表面有水膜存在时,钢中不同组分之间表现出不同的电位(期间存在电位差)水膜是离子导体,金属本身是电子导体,具备了腐蚀电池的条件(比如碳素体为阴极、奥式体为阳极) 。无数类似“微电池”运行的结果,钢表面就“生锈”了。
![]()
如果能理解金属成分(组分)对于形成“微电池”的影响与作用,就不可以解释为什么金属纯度越高耐腐蚀性能就越好的道理。金属纯度越高,说明杂质越少、越单一。形成“微电池”的机会、数量也就越少。那当然就比较耐腐蚀了。通常的铝合金常常用一层纯铝包覆,正是为了提高铝合金的耐蚀性,这也是借助减少“微电池”生成这一原理,提高防护性能的应用实例。