维权声明:本文为54943110原创作品,本作者与仪器信息网是该作品合法使用者,该作品暂不对外授权转载。其他任何网站、组织、单位或个人等将该作品在本站以外的任何媒体任何形式出现均属侵权违法行为,我们将追究法律责任。
导读:在正文之前,我首先说说为什么写这个文章以及整篇文章的构思过程。☆ 前几天我在论文写作与投稿板块中回了个帖子,阐述了我对于论文选题的理解,八个字:小题大做,大题小做http://bbs.instrument.com.cn/shtml/20110929/3560922/ 这里我通过这篇文章诠释下小题大做的含义。这个一般是指对于某一个点或者是测试中的某个条件的深入挖掘。小题指的是研究范围的极有限性,大做则是针对研究深度而言。当然我这里只是抛砖引玉一下,利用几年的原始数据做一个分析。论文质量如何等待各位专家鉴定☆ 整篇文章是针对应急监测中发光菌急性毒性测试的。很多人认为这个测试的数据偏差较大,重复性低。其实,很多时候是我们对实验材料或者是过程的掌握不够,同时国标也不是很完善(毕竟1995年的国标了,技术上更多的是抄袭,近年应该会出新的HJ的,到时候应该会有所更新)☆ 对于论文的构思,主要是基于对生物试验中阴性对照和阳性对照的理解,加入了统计分析,一切用数据说话。文章中还有另外一个创新点就是对于军也初始发光强度范围的确定。为什么要去做这个分析呢?我们在测试过程中发现,有时候还没做实验其实你的实验材料已经没啥活性了。若不及时发现,可能导致实验失败,甚至出现错误数据。对于具体测试方法的改进,不是一两句话能说明白的,我将另出一文加以详细阐述
基于多级控制的急性毒性测试质控手段
摘要:本文通过试验研究了以费舍尔弧菌(Vibrio fischeri)为受试生物的生物毒性测试质量控制方法,确定了菌液原始发光值和实验空白光损率对测定结果的影响以及阳性对照物控制范围。结果表明:为使测试结果有更高的重现性,菌液初始发光强度应大于500000;实验空白光损率应保持在50%±10%范围内;1.07mg/L的Zn2+溶液阳性对照质控样应该控制在51%±11%范围内。
关键词:费舍尔弧菌 生物毒性 质量控制
Study on Multi-level data quality control of
luminescent bacteria toxicity text
Abstract: This paper studies the quality control methods for luminescent bacteria toxicity text using Vibrio fischeri,including the original bacilli blank light-emitting and experimental results on the determination of loss rate and the positive control of the control range. The results showed that: To make the test more reproducible, the initial luminous intensity should be greater than bacilli 500000; the blank optical loss rate should be maintained at the range of 50% ± 10%; the result of the test for 1.07mg / L of Zn2+ positive solution should be controlled at the range of 51% ± 11%.Key words: Vibrio fischeri, biotoxicity, quality control 在环境污染物的毒性评价和监测中,发光细菌法是一种具有快速、灵敏和廉价等优点的直接生物测试方法[1-3]。理化和生物有毒物质会影响发光菌的呼吸作用、电子传输系统、ATP产生、蛋白质或 脂类合成,从而改变发光强度[4]。发光菌急性毒性测试系统就是利用此原理对水样的生物毒性进行分析。目前,发光菌急性毒性测试的研究仅局限于以明亮发光杆菌T3小种(Photobacterium phosphoreum T3)为受试生物的阳性对照选择上[5],对其他微生物的质量控制研究也主要以规范操作和实验室管理为主[6-8],对Vibrio fischeri急性毒性测试质量控制方面的研究较少。这使得Vibrio fischeri急性毒性测试的重现性不高[9],制约了仪器的推广应用和相关技术的发展。通过实验分析以费舍尔弧菌为受试生物的急性毒性测试系统的质量控制方法,进而使生物毒性的实验数据更具可靠性和可重复性,为管理部门的决策提供更为科学的决策依据。1.实验材料和仪器 Vibrio fischeri(干粉):购自美国SDI公司 Delta-tox急性毒性系统(美国SDI公司) Tox-screen Ⅱ毒性分析仪(以色列Check-light公司) Zn2+阳性对照溶液:由ZnSO4·7H2O加蒸馏水水配置,浓度1.07mg/L2.实验方法: Vibrio fischeri发光菌冻干粉由美国SDI公司提供,用Delta-tox急性毒性检测系统的81.9%低毒性样本测试方法[10]进行毒性测试。菌液的发光强度用Tox-screen Ⅱ毒性分析仪测定。 取出储存在-20 ℃下的冻干细菌,立即加入0.3ml稀释液让细菌水合。 20分钟后,摇匀,用Tox-screen Ⅱ毒性分析仪测定菌液原始发光强度,记为I0。取出0.1ml,测定菌液发光强度,记为I1(用于对照的记为I1’);加入0.9ml经渗透压调解的水样(对照为纯水),反应5min后,测定菌液发光强度,记为I2(对照为I2’)。水样毒性的变化用相对抑制率表示,当样品中存在刺激发光物质时,相对抑制率以正值表示:各处理段水样毒性的变化用相对抑制率表示,当样品中存在刺激发光物质时,相对抑制率以负值表示。![]() 3.实验结果与讨论3.1 菌液原始发光值的对实验结果的影响 Vibrio fischeri发光菌活化后的原始发光值是反映该菌活化效果的指标之一。健康的菌种在活化后都具有较高的发光强度。反之,活菌含量少或活化剂中含有少量有毒物质菌液活化后的原始发光值就会降低。 对55支Vibrio fischeri发光菌分析得,其初始发光值的Kolmogorov-Smirnov正态性检验sig为0.200,大于0.05,如图1所示。所以,在95%置信区间下,发光菌初始发光值频次分布呈正态分布。RLU均值1.04×106。 用该55支Vibrio fischeri发光菌对1.07mg/L的Zn2+溶液[5]进行测试,结果如图2所示。当菌液初始发光强度大于500000时,测试结果均值在50%左右,且偏差较小,在4%~7%之间;当菌液初始发光强度在200000~500000之间时均值虽然在50%~61%之间,但偏差较大,为15%~33%,这可能是由于菌液活性偏低,使得对同一浓度污染物的反应不一致;当菌液初始发光强度小于200000时,测试均值接近100%,此时菌液活性较弱。因此,为提高测试结果的重现性,应使菌液初始发光强度保持在500000以上,如过低则应重新测定。
3.实验结果与讨论3.1 菌液原始发光值的对实验结果的影响 Vibrio fischeri发光菌活化后的原始发光值是反映该菌活化效果的指标之一。健康的菌种在活化后都具有较高的发光强度。反之,活菌含量少或活化剂中含有少量有毒物质菌液活化后的原始发光值就会降低。 对55支Vibrio fischeri发光菌分析得,其初始发光值的Kolmogorov-Smirnov正态性检验sig为0.200,大于0.05,如图1所示。所以,在95%置信区间下,发光菌初始发光值频次分布呈正态分布。RLU均值1.04×106。 用该55支Vibrio fischeri发光菌对1.07mg/L的Zn2+溶液[5]进行测试,结果如图2所示。当菌液初始发光强度大于500000时,测试结果均值在50%左右,且偏差较小,在4%~7%之间;当菌液初始发光强度在200000~500000之间时均值虽然在50%~61%之间,但偏差较大,为15%~33%,这可能是由于菌液活性偏低,使得对同一浓度污染物的反应不一致;当菌液初始发光强度小于200000时,测试均值接近100%,此时菌液活性较弱。因此,为提高测试结果的重现性,应使菌液初始发光强度保持在500000以上,如过低则应重新测定。![]()
![]()
图2 菌液初始发光值对测试结果的影响
3.2 实验空白光损率对实验结果的影响![]()
图3 实验空白光损率分布情况
由图3可知,加入纯水后按样品分析步骤测定,发光菌菌液的发光强度较刚活化完的时候低。平均光损率50%,偏差5%。由于这几组实验空白对应的阳性参照相对偏差在10%之内,且在不同温度下完成,所以在95%置信区间下,实验空白光损率应保持在50%±10%范围内。通常情况下,实验空白的光损率不会低于40%,若实验空白光损率小于40%,则应检查测定温度是否合适[4],或其他测定过程是否存在失误;若实验空白的光损率大于60%,则应首先检查实验用水是否受污染。必要时应重新活化发光菌进行测定。3.3 阳性对照物控制范围的确定 由于Zn2+是一种无色离子,其发光菌急性毒性较Hg2+的小且稳定,此外在较大pH范围内,形态相对单一[5],所以Zn2+更适合作为发光菌急性毒性测试的阳性对照物。 取初始发光强度在500000以上的发光菌为受试生物,对45组以1. 07mg/L的Zn2+溶液测试结果统计得,测试结果均值51%,偏差5.5%。所以在95%置信区间内,1.07mg/L的Zn2+溶液阳性对照质控样应该控制在51%±11%范围内。若超出此范围,应考虑测试条件是否在合适的范围内[4]。4 结论 在95%置信区间下,发光菌初始发光值频次分布呈正态分布。为使测试结果有更高的重现性,菌液初始发光强度应大于500000;实验空白光损率应保持在50%±10%范围内;1.07mg/L的Zn2+溶液阳性对照质控样应该控制在51%±11%范围内。若上述质控数据偏离范围,则应分别考虑菌液活性、试剂是否受污染、温度等测试条件是否在合适范围内,必要时应取新的Vibrio fischeri(干粉)重新测定。
参考文献[1] 韦东普,马义兵,陈世宝. 应用淡水发光细菌测定土壤Cu急性毒性的影响因素研究[J]. 农业环境科学学报.2009,7:1386-1391[2]T.Campisi, F.Abbondanzi, C.Casado-Martinez. Effect of sediment turbidity and color on light output measurement for microtox basic solid-phase test [J].Chemosphere,2005(1):9-15[3] 贺志庆,王文波.发光菌特性及其在环境监测方面的应用[J].化学工程与设备.2008,7:105-106[4] 赵洋甬,胡建林,邵立军. 发光菌毒性测试的影响因子研究[J]. 现代科学仪器.2010,3:75-78[5] 王丽莎,魏东斌,胡洪营. 发光细菌毒性测试条件的优化与毒性参照物的应用[J].环境科学研究,2004,17(4):61-62[6] 孙晶秋.微生物检验质量管理里存在的问题及对策[J].中外医疗.2009,16:117[7] 王国洪.微生物检验质量影响因素分析[J].中国农村医学杂志.2008,6(2):58-59[8] 杨美琴,孙来玉,王凤云.微生物实验室质量控制与管理[J].职业与健康.2008,24(2):126-127[9] 何芬,李子龙,晏恒等.水质毒性检测方法的比对研究[J]. 环境科学与管理.2008,11(33):128-130[10] ISO 11348-3:2007,水质-有关费歇尔弧菌属的光发射水样品的抑制效果的测定(发光细菌试验)[11] 陈洪斌,东刘成,唐贤春.受污染水源水生物处理中微型后生动物的研究[J].中国环境科学.2008,28(12):1105-1110最后,上几张漂亮的照片(部分来自网络)
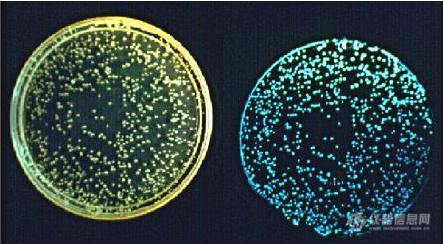
![]()
上图左边是正常光照情况下琼脂干版上的费氏弧菌的生物发光量,右边的是黑暗条件下的生物发光量
我们正是利用其黑暗条件下的发光行为进行测试的
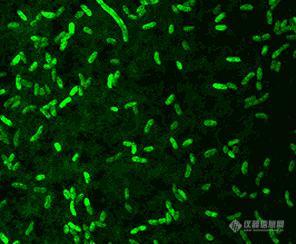
![]()
上图是通过荧光标记拍摄得到的费氏弧菌照片
图片更新待续