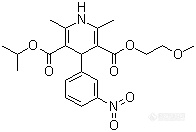
尼莫地平滴定的方法是:
取本品约0.18g,精密称定,加无水乙醇25ml,微温使溶解,加高氯酸溶液(取70%高氯酸溶液8.5ml,加水至100ml)25ml,加邻二氮菲指示液4滴,用硫酸铈滴定液(0.1mol/L)滴定至溶液由橙红色变为浅黄绿色,并将滴定结果用空白试验校正。
每1ml硫酸铈滴定液(0.1mol/L)相当于20.92mg C21H24N2O7。
该滴定是氧化还原吗?那么高氯酸是和尼莫地平的NH反应的吗?那么硫酸铈和什么反应呢
因为我们现在要测定尼莫地平杂质对照品的含量,想依法算出其滴定度,但是不了解其反应式?
请大家帮个忙
![]()