粉防己碱药理作用及测定方法
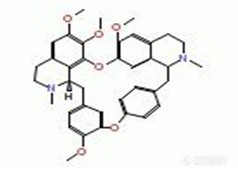
粉防己碱 (汉防己甲素,tetrandrine,Tet)是从千金藤属防己科植物粉防己(Stephaniaterandra S.Moore) 的干燥块根中提取的一种主要活性成分,化学结构属双苄基异喹啉类化合物[1]。近年来 ,国内外对其药理作用机制进行了较为广泛的研究。资料表明,Tet的抗心律失常、抗高血压、抗炎、抗肿瘤多药耐药性等作用均与其直接或间接拮抗钙通道和钙调蛋白有关 ,而且发现其在抗肝、肺纤维化方面有较强活性。其免疫机能调节及肿瘤防治等方面具有很好的应用景。
1 粉防己碱药理作用
1.1 心血管系统的作用
(1) 抗心律失常:Tet可拮抗哇巴因及氯化钙诱发的心律失常 ,但对乌头碱及电刺激引起的心律失常拮抗作用较弱或不明显。其作用机制与维拉帕米相似 ,与拮抗Ca2+内流有关。
(2) 抗心肌缺血、缺氧及再灌注损伤[2]:Tet可减轻大鼠工作心脏缺血再灌注心肌损伤 ,促进冠脉流出液、心输出量的恢复 ;防止左心室舒张末期压和等容舒张左室内压下降时间常数的升高 ;抑制肌酸激酶释放 ,维持心肌线粒体Ca2+ 稳态,表明Tet尤对心肌舒张功能和冠脉循环的保护为优。
(3) 降压作用:Tet可显著降低自发性高血压大鼠的平均动脉压 ,抑制主动脉平滑肌的持续性收缩。还有助于慢性肺源性心脏病时肺动脉高压的降低和肺腺泡内动脉构型改善[3]。
1.2 脑缺血缺氧作用 Tet可显著提高脑细胞对缺血缺氧的耐受性。Ca2+超负荷可导致大脑细胞损伤 ,细胞线粒体内Ca2+聚集致氧化磷酸化受阻 ,导致三磷酸腺苷 (ATP)耗竭 ; Ca2+激活蛋白酶和磷酸脂酶而破坏结构的完整性 ,加重脑细胞的损伤 ,加之乳酸中毒使脑细胞膜和血管通透性增加 ,引起细胞毒性脑水肿。Tet作为钙拮抗剂可阻止Ca2+ 内流 ,减轻脑水肿 ,一定程度上逆转了上述病理过程 ,对脑缺血损伤有明显的保护作用[4-5]。
1.3 抗缺血再灌注肾损伤作用[5] Tet对大鼠急性缺血再灌注肾损伤有保护作用 ,能明显降低血清肌酐和尿素氮水平。其机制是Tet直接或通过抑制钙离子内流而间接抑制磷脂酶A2(PLA2)活性 ,影响花生四烯酸 (AA)及其代谢产物释放 ,减少多种炎症介质合成 ,改善肾脏血流动力学 ,增加肾损伤大鼠的肾小球滤过率和肾血浆流量而发挥作用。近年发现Tet在急性缺血肾损伤过程中可通过降低肾小管上皮细胞凋亡 ,达到减轻肾组织细胞损伤 ,促进肾组织修复的作用[6]。
1.4 抗血小板聚集及凝血作用该作用可能与其抑制Ca2+ 内流和内源性PAF释放有关 ,间接或直接阻止了血小板活化的第三种途径。Tet能抑制血小板和多形核白细胞合成血栓素A2 (TXA2),也能减少兔全血TXB2的产生 ,可能通过抑制内源性AA的释放减少TXA2的生成。Tet在体外可促进家兔纤维蛋白溶解和抑制凝血酶引起的血液凝固过程 ,抑制血栓形成。
1.5 调节机体免疫机能临床上,植物粉防己常被用于治疗类风湿关节炎等自身免疫性疾病,其主要生物活性成分Tet具有很强的免疫调节功能。研究表明Tet通过下调T细胞蛋白激酶C信号转导通路,抑制T细胞增殖,减少IL2的分泌及下调T细胞激活抗原CD71的表达。Tet可剂量依赖性抑制内毒素、PMA及二氧化硅诱导肺泡巨噬细胞的NFκB激活及NFκB依赖报告基因的表达,但对核转录因子SP1的DAN结合活性及SP1依赖报告基因的表达无影响,这一作用与抑制IκB降解的某些信号转导通路、清除羟自由基有关[11-12]。
1.6 抑制增生性瘢痕 Tet能有效抑制瘢痕成纤维细胞与胶原基质网的收缩效应 ,可能机制是 :①Tet能有效阻断Ca2+ 跨膜内流 ,降低Ca2+ 浓度 ,同时抑制磷酸肌醇第二信使系统促肌浆网Ca2+的释放而发挥作用 ;②Tet能影响活性因子作用于成纤维细胞 ,从而阻断α平
滑肌肌动蛋白在成纤维细胞中的表达。
1.7 抗肿瘤多药耐药性 Tet可逆转肿瘤多药耐药性, 有较好临床应用前途的化疗增效剂。肿瘤细胞对结构不同 ,作用方式不同的多种抗癌药物产生的耐药性成为肿瘤化疗的一大障碍。Tet具有钙拮抗作用 ,可能干扰Pgp的药物外排机制 ,在体内外均能逆转Pgp介导的MDR。
1.8 防治消化系疾病作用
(1) 抗肝纤维化 Tet能有效的治疗肝纤维化 ,其机制在抑制储脂细胞的增殖分化 ,减少Ⅳ型胶原在肝组织中的沉积。体外研究实验表明 , Tet对肝细胞、储脂细胞的DNA及胶原合成有明显抑制作用,促进RBL肝细胞生长增殖 ,但抑制了3T6成纤维细胞增殖 ,此作用与阻断Ca2+内流无关[6-7]。
(2) 降低门静脉高压门静脉高压是各种原因所致肝硬化的主要临床表现。临床研究表明Tet能够显著减低肝硬化患者门静脉压力,减少门静脉血流量,降低食管曲张静脉压力;连续用药患者2年内无再次出血率达87.6%,疗效显著显著优于安慰剂、硝苯地平及维拉帕米。
1.9 其他作用 Tet可显著降低脑组织Ca2+及MDA含量,减轻大脑皮质及海马超微结构的改变;显著抑制小鼠实验性过敏性结合膜炎,降低疱疹病毒性角膜炎的发生率;减轻四氧嘧啶胰岛细胞损害程度,抑制实验性糖尿病的发生。
2 含量测定方法:近年来,人们采用很多方法检测药用植物及其制剂中粉防己碱的含量。现将各种方法介绍如下:
(1) 薄层紫外分光光度法
采用硅胶G薄层板,展开剂:氯仿-丙酮(2:1)。供试品溶液的制备:取样品4g,置索氏提取器内,用甲醇回流提取3h,滤入100mL量瓶中,加甲醇至刻度,即得。于242nm处测定吸收度。测得粉防己中粉防己碱的含量在0.15%~0.24%之间,回收率103.65%,RSD为1.59(n=6)。
(2) 薄层扫描法
马俊玲等采用薄层扫描法测定祛风合剂中粉防己碱的含量。吸附剂:硅胶G 0.5%羧甲基纤维素钠薄层板;展开剂:苯- 丙酮- 二乙胺(8∶1∶0.3);显色剂:稀碘化铋钾试液;扫描方式:双波长反射式锯齿扫描;检测波长λS=500nm,λR=650 nm;狭缝:0.4 mm×0.4 mm;线性参数:SX=3;灵敏度:中。精密称取粉防己碱对照品4.90mg,加甲醇溶解、定容至5mL,制成0.98gL-1的溶液,作为对照品溶液。。测得粉防己碱的含量在线性范围为0.98~4.9ug(r=0.9956)内良好,平均回收率为97.45%, RSD为1.24%。
(3) 高效毛细管电泳-高频电导检测法[8]
王峻梅等建立了植物粉防己中生物碱测定的毛细管电泳高频电导法,采用非接触式毛细管电泳高频电导检测装置,避免了电化学检测中电极与溶液直接接触,以融硅毛细管(150um×60cm)为分离柱,1mmoLHAC+2mmoLNH4AC +10moLLβCD+2mmoLSDS缓冲液为电泳介质,分离电压14.0kV,用高频电导法检测,考察了缓冲液的种类、浓度、添加剂、分离电压和进样量对分离和检测的影响;在优化条件下的线性范围分别为:粉防己碱12.5~900ug.mL-1;检出限为:粉防己碱6.25 ug.mL-1;样品加标回收率分别为92.7%~98.9%。
(4) 高效液相色谱法[9]
和健等采用高效液相色谱法测定了迪可颗粒[10](赤芍、防己、红花、山药等)中粉防己碱的含量。色谱柱为diamonsil ODS(5um,250mm×4.6mm)分析柱;流动相:甲醇-乙腈-0.003moL.L-1-KHPO4-二乙胺(55:25:20:0.06),检测波长230nm;流速为1.0mL·min-1。称取本品0.3g于25mL量瓶中,加氨试液8滴,加塞放置30 min。加醋酸乙酯近刻度,超声1h,放冷后加醋酸乙酯至刻度,摇匀。取上清液10mL,水浴蒸干,残渣加3∶2的甲醇水溶液转移至5mL量瓶,稀释至刻度,过0.45um的滤膜,即得供试品溶液;精密称取粉防己碱对照品适量加入3∶2的甲醇水制成4 ug.mL-1的溶液,作为对照品溶液。测得粉防己碱0.0278~0.2227ug范围内峰面积和进样量呈良好的线性关系,r=0.9999,平均回收率为98.38。
综上所述,有关粉防己碱的药理学研究进行得广泛且较深入,其含量测定也是方法众多,高效液相色谱法简便、快速、准确,是目前的应用趋势。对于粉防己碱,更有待于进一步研究。
参考文献
[1] 中华人民共和国卫生部药典委员会.中华人民共和国卫生部药品标准中药成方制剂.第十九册..1998.135.
[2] 李庆平,杨解人,铙曼人.预先给予粉防己碱对大鼠工作心脏缺血在灌住损伤的保护作用[J].中国药理学与毒理学杂志,1994,8(2):114.
[3] 李凤前,陆彬.粉防己碱抗肺动脉高压研究进展[J].中国师,2000,3(2):77.
[4] 祝武强,曾秋棠,曹林生,等.粉防己碱对缺氧和复氧损伤心室肌细胞内Ca2+超载的作用[J].临床心血管病杂志,2000,16(2):83.
[5] 祯晓光,顾丽英,陈桂英,等.粉防己碱对鼠脑缺血的作用[J].中国药理学通报,1997,13(2):148.
[6] 郝俊文,孙成春,张 莉etal.汉防己甲素对硫唑嘌呤致大鼠肝损伤的保护作用.中国临床药理学与治疗学杂志,1997;2(3):180~2.
[7] 孙自勤,王要军,权启镇,张志坚.汉防已甲素与秋水仙碱抗肝纤维化作用的比较.中国药理学通报,1996;12(4):345~719(2):179~81.
[8] 王天勇,杨文远.分析测试技术与仪器,1995,1(1):31.
[9] 张云,宋旭峰.高效液相色谱法测定轻身减肥片中大黄素与大黄酚的含量[J]..中国实验方剂学杂志,2002,8(5):46.
[10] 林启寿.中草药成分化学[M]..北京:科学出版社.1997.742.
[11] Song Q, Baxter GD, Kovacs EMet al.Inhinition of apoptosis in human tumour cells by okadaic acid.J Cell Physiol,1992;153(3):550~6.
[12] He QY, Meng FH, Zhang HQ. Reduction ofdoxorubicin resis-
tance by tetrandrine and dauricine inharringtonine-resistant humanleukemia (HL60) cells.Acta Pharmacologica Sinica,1996;17.