原文由 comeet(comeet) 发表:
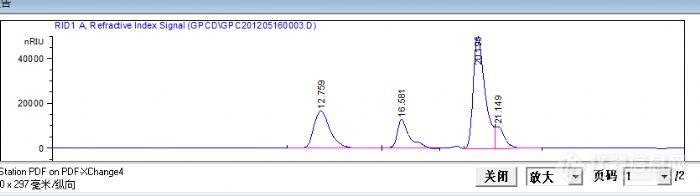
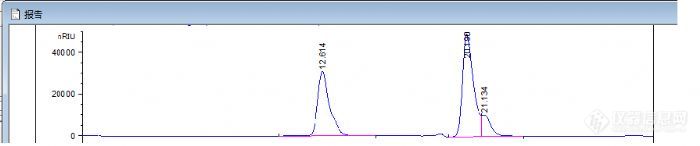
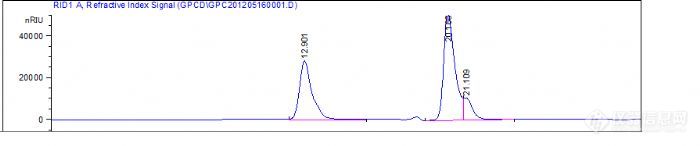
谢谢小不董的热心回答,回去看了下第一个图,是我截图错了,这个是6000和10000还有另一个H0-PEG24-OH 混合后进样的图。
我的柱子是agilent 的 PL aquagel-OH 5um 20, 300*7.5mm MW Range 100 to 10000.耐纯水的,两根串联。
有几个问题想请教下:
1,样品我是用流动相配制的,为什么能确定20min出来的是溶剂峰呢?
2,我要分析的是PEG系列的多分散聚合物,如果用纯水一般加什么盐,加多少比较好呢?
3,多分散的样品,以我的理解应该会出一系列正态分布的峰吧,为什么只出一个啊?谢谢了
原文由 小不董(doxw0323) 发表:原文由 comeet(comeet) 发表:
谢谢小不董的热心回答,回去看了下第一个图,是我截图错了,这个是6000和10000还有另一个H0-PEG24-OH 混合后进样的图。
我的柱子是agilent 的 PL aquagel-OH 5um 20, 300*7.5mm MW Range 100 to 10000.耐纯水的,两根串联。
有几个问题想请教下:
1,样品我是用流动相配制的,为什么能确定20min出来的是溶剂峰呢?
2,我要分析的是PEG系列的多分散聚合物,如果用纯水一般加什么盐,加多少比较好呢?
3,多分散的样品,以我的理解应该会出一系列正态分布的峰吧,为什么只出一个啊?谢谢了
由于你的柱子的range是100to10000,所以在分离6000,10000不是很好,10000已经是他的分析极限了,但能把6000和HO-PEG24-OH分离得很好,所以建议你可以考虑使用PL aquagel-OH 30 10um,300*25mm的柱子,他分析极限是100-30000。part no; 1220-6130。
你使用的这个柱子和我推荐的这个柱子都可以用纯水,你只分析PEG的话,可以不加缓冲盐都可以,但如果你分析含有anionic阴离子的高分子,要价0.1-0.3M NaNO3 和pH=7-9 0.01M NaH2PO4,若含有cationic阳离子的,建议使用0.2-0.8M NaNO3 和pH=7-9 0.01M NaH2PO4,也都可以再加甲醇最多到50%比率的水溶液做流动相。
原文由 shawnkmchen(shawnkmchen) 发表:原文由 小不董(doxw0323) 发表:原文由 comeet(comeet) 发表:
谢谢小不董的热心回答,回去看了下第一个图,是我截图错了,这个是6000和10000还有另一个H0-PEG24-OH 混合后进样的图。
我的柱子是agilent 的 PL aquagel-OH 5um 20, 300*7.5mm MW Range 100 to 10000.耐纯水的,两根串联。
有几个问题想请教下:
1,样品我是用流动相配制的,为什么能确定20min出来的是溶剂峰呢?
2,我要分析的是PEG系列的多分散聚合物,如果用纯水一般加什么盐,加多少比较好呢?
3,多分散的样品,以我的理解应该会出一系列正态分布的峰吧,为什么只出一个啊?谢谢了
由于你的柱子的range是100to10000,所以在分离6000,10000不是很好,10000已经是他的分析极限了,但能把6000和HO-PEG24-OH分离得很好,所以建议你可以考虑使用PL aquagel-OH 30 10um,300*25mm的柱子,他分析极限是100-30000。part no; 1220-6130。
你使用的这个柱子和我推荐的这个柱子都可以用纯水,你只分析PEG的话,可以不加缓冲盐都可以,但如果你分析含有anionic阴离子的高分子,要价0.1-0.3M NaNO3 和pH=7-9 0.01M NaH2PO4,若含有cationic阳离子的,建议使用0.2-0.8M NaNO3 和pH=2-7 0.01M NaH2PO4,也都可以再加甲醇最多到50%比率的水溶液做流动相。
您好,借此宝地咨询一下,我最近在做水相的GPC,需要测试阴离子和阳离子型高分子的分子量。想请教一下,对于阴离子加入0.1-0.3M的NaNO3是为了屏蔽电荷吧?用0.01M NaH2PO4 调节pH到7-9也是为了去质子化减少电荷量吧?那么为什么阳离子型的需要更高的离子强度来屏蔽电荷呢?像季铵盐类的水性高分子,为什么也要调节pH值呢?后面加入甲醇(我看到也有加乙腈之类的)的目的是什么呢?十分期待您的答复!!!万分感谢!!!
原文由 小不董(doxw0323) 发表:原文由 shawnkmchen(shawnkmchen) 发表:原文由 小不董(doxw0323) 发表:原文由 comeet(comeet) 发表:
谢谢小不董的热心回答,回去看了下第一个图,是我截图错了,这个是6000和10000还有另一个H0-PEG24-OH 混合后进样的图。
我的柱子是agilent 的 PL aquagel-OH 5um 20, 300*7.5mm MW Range 100 to 10000.耐纯水的,两根串联。
有几个问题想请教下:
1,样品我是用流动相配制的,为什么能确定20min出来的是溶剂峰呢?
2,我要分析的是PEG系列的多分散聚合物,如果用纯水一般加什么盐,加多少比较好呢?
3,多分散的样品,以我的理解应该会出一系列正态分布的峰吧,为什么只出一个啊?谢谢了
由于你的柱子的range是100to10000,所以在分离6000,10000不是很好,10000已经是他的分析极限了,但能把6000和HO-PEG24-OH分离得很好,所以建议你可以考虑使用PL aquagel-OH 30 10um,300*25mm的柱子,他分析极限是100-30000。part no; 1220-6130。
你使用的这个柱子和我推荐的这个柱子都可以用纯水,你只分析PEG的话,可以不加缓冲盐都可以,但如果你分析含有anionic阴离子的高分子,要价0.1-0.3M NaNO3 和pH=7-9 0.01M NaH2PO4,若含有cationic阳离子的,建议使用0.2-0.8M NaNO3 和pH=2-7 0.01M NaH2PO4,也都可以再加甲醇最多到50%比率的水溶液做流动相。
您好,借此宝地咨询一下,我最近在做水相的GPC,需要测试阴离子和阳离子型高分子的分子量。想请教一下,对于阴离子加入0.1-0.3M的NaNO3是为了屏蔽电荷吧?用0.01M NaH2PO4 调节pH到7-9也是为了去质子化减少电荷量吧?那么为什么阳离子型的需要更高的离子强度来屏蔽电荷呢?像季铵盐类的水性高分子,为什么也要调节pH值呢?后面加入甲醇(我看到也有加乙腈之类的)的目的是什么呢?十分期待您的答复!!!万分感谢!!!
不好意思, 我写错了,误导了你,含有阳离子的用pH=2-7的0.01M NaH2PO4来调节。目的是为了都是为了减小化学键的作用,让高分子有机物能自由穿过柱子,只受到体积排阻的作用。加甲醇的目的或作用有两个,一个是抑制细菌的生长,一个也是减小化学键的作用。