材料和方法
一、标本来源
收集2011年4月—2014年4月间本市第一人民医院及本市一县人民医院门诊和病房收集的发热(体温≥38℃)伴咳嗽或咽痛的咽拭子标本,在4~8℃条件下保存,并在24小时内冷藏送至流感实验室,尽快分离接种,未能及时接种存-70℃保存。
二、试验方法
1、病毒分离与鉴定:标本经常规处理后,接种到生长状态良好的传代犬肾(MDCK)细胞,连续观察细胞病变,并进行血球凝集试验,对于血凝滴度小于1:16的毒株,将病毒培养液进行10-1—10-3稀释后进行传代。收获的病毒培养液用人O型红细胞进行血凝素(HA)试验,确定病毒滴度。然后采用国家流感中心的各型别/亚型标准参照血清进行血凝抑制(HI)试验,确定病毒的型别和亚型。
2、病毒Real-time one step RT-PCR检测
2、1使用ambion公司生产的Mag MAXTM—96Viral RNA Isolation Kit,按照病毒RNA提取试剂盒说明书提取标本中的病毒RNA。
2、2 PCR,按照AB公司的Ag Path—IDTM One—Step RT—PCR Kit 试剂盒说明书操作。扩增条件:45℃ 10分钟1个循环,95℃ 10分钟1个循环,95℃ 15秒钟,60℃ 45秒钟40个循环收集荧光。
三、结果
1、病毒分离结果 2011年1月至2013年12月本市共采集咽拭子标本2780份。分离和鉴定确认的流感病毒87株,病毒分离阳性率3.13%,其中H1N1亚型流感病毒16株,占18.39%,H3N2亚型5株,占5.75%,B型中yamagata系16株,占18.39%,B型中victoria系50株,占57.47%。
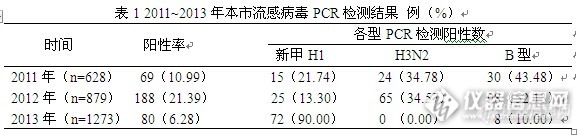
2、PCR检测结果 2011年1月至2013年12月本市共采集咽拭子标本2780份。PCR检测阳性标本337份,检测阳性率为12.12%。其中新甲H1亚型流感病毒112份,占33.23%,H3N2亚型89份,占26.41%,B型136份,占40.36%。2011~2013年流行期,以B型流感病毒占优势,H3N2亚型为弱势。
![]()