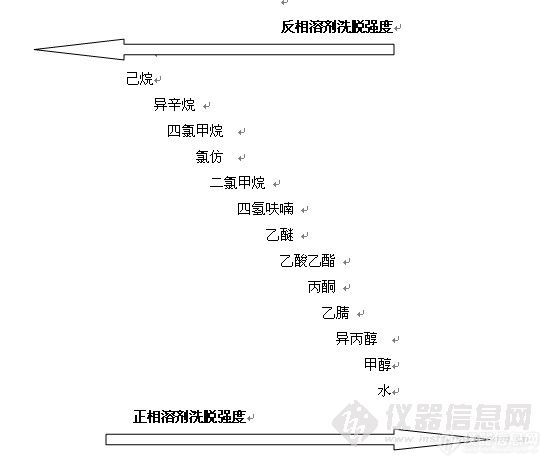
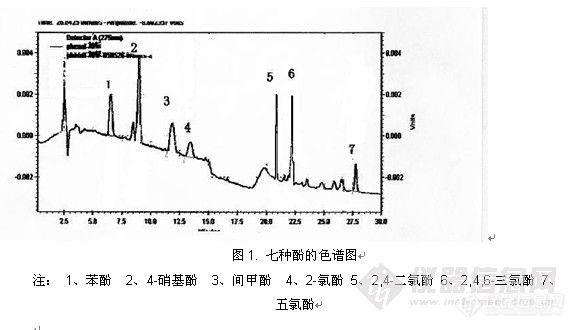
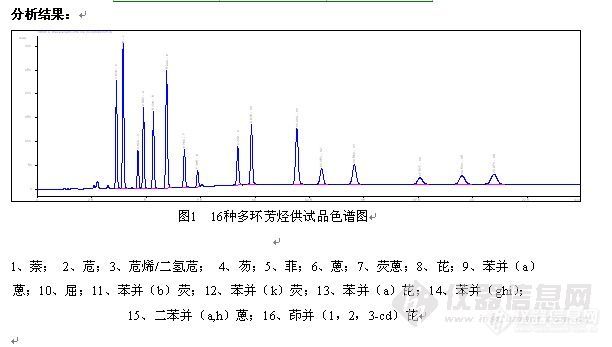
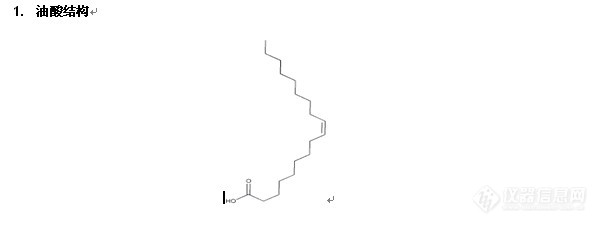
固相萃取技术原理及应用
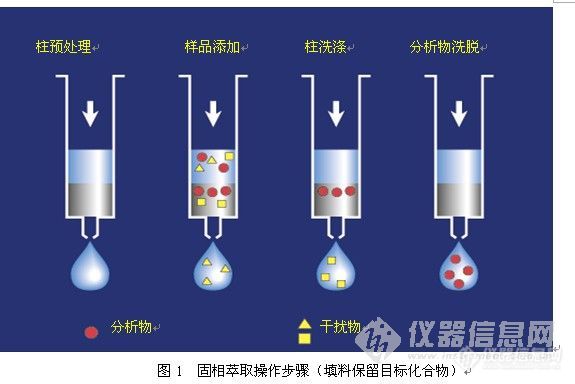
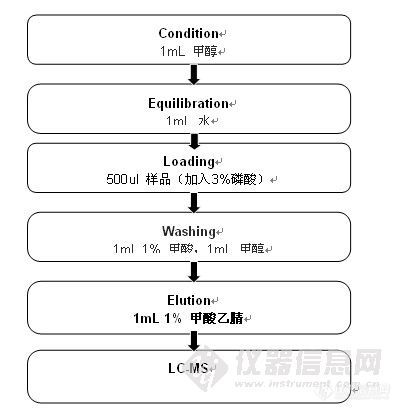
一、固相萃取基本原理与操作 1、固相萃取吸附剂与目标化合物之间的作用机理固相萃取主要通过目标物与吸附剂之间的以下作用力来保留/吸附的1)疏水作用力:如C18、C8、Silica、苯基柱等2)离子交换作用:SAX, SCX,COOH、NH2等3)物理吸附:Florsil、 Alumina等2、p H值对固相萃取的影响pH值可以改变目标物/吸附剂的离子化或质子化程度。对于强阳/阴离子交换柱来讲,因为吸附剂本身是完全离子化的状态,目标物必须完全离子化才可以保证其被吸附剂完全吸附保留。而目标物的离子化程度则与pH值有关。如对于弱碱性化合物来讲,其pH值必须小于其pKa值两个单位才可以保证目标物完全离子化,而对于弱酸性化合物,其pH值必须大于其pKa值两个单位才能保证其完全离子化。对于弱阴/阳离子交换柱来讲,必须要保证吸附剂完全离子化才保证目标物的完全吸附,而溶液的pH值必须满足一定的条件才能保证其完全离子化。3、固相萃取操作步骤及注意事项针对填料保留机理的不同(填料保留目标化合物或保留杂质),操作稍有不同。1)填料保留目标化合物固相萃取操作一般有四步(见图1):Ø 活化---- 除去小柱内的杂质并创造一定的溶剂环境。(注意整个过程不要使小柱干涸)Ø 上样---- 将样品用一定的溶剂溶解,转移入柱并使组分保留在柱上。(注意流速不要过快,以1ml/min为宜,最大不超过5ml/min)Ø 淋洗---- 最大程度除去干扰物。(建议此过程结束后把小柱完全抽干)Ø 洗脱---- 用小体积的溶剂将被测物质洗脱下来并收集。(注意流速不要过快,以1ml/min为宜)
如下图1: ![]() 2)填料保留杂质固相萃取操作一般有三步(见图2):Ø 活化--除去柱子内的杂质并创造一定的溶剂环境。(注意整个过程不要使小柱干涸)Ø 上样--将样品转移入柱,此时大部分目标化合物会随样品基液流出,杂质被保留在柱上,故此步骤要开始收集(注意流速不要过快)Ø 洗脱---用小体积的溶剂将组分淋洗下来并收集,合并收集液。(注意流速不要过快)此种情况多用于食品或农残分析中去除色素。
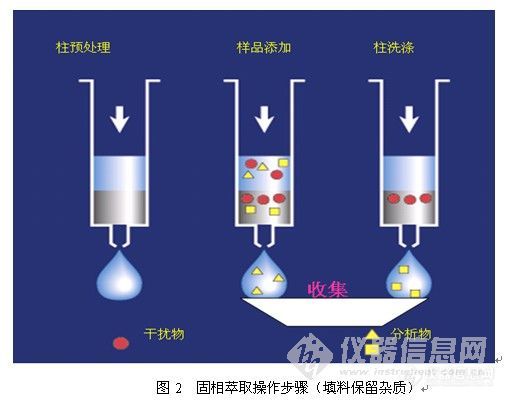
2)填料保留杂质固相萃取操作一般有三步(见图2):Ø 活化--除去柱子内的杂质并创造一定的溶剂环境。(注意整个过程不要使小柱干涸)Ø 上样--将样品转移入柱,此时大部分目标化合物会随样品基液流出,杂质被保留在柱上,故此步骤要开始收集(注意流速不要过快)Ø 洗脱---用小体积的溶剂将组分淋洗下来并收集,合并收集液。(注意流速不要过快)此种情况多用于食品或农残分析中去除色素。
如下图2:
![]()
二、固相萃取方法的建立与优化
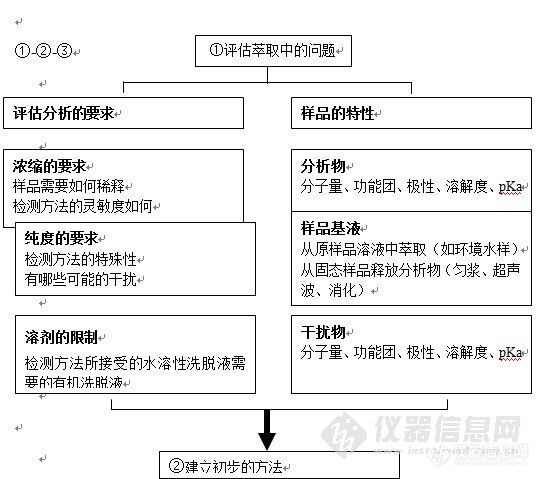
固相萃取技术使用起来虽然比液液萃取简单,但建立一个固相萃取的方法并无快捷方式可走。建立固相萃取方法必须考虑与萃取过程相关的多种因素,归纳起来可通过下图来了解:
方法建立如下图片1.jpg:
![]()
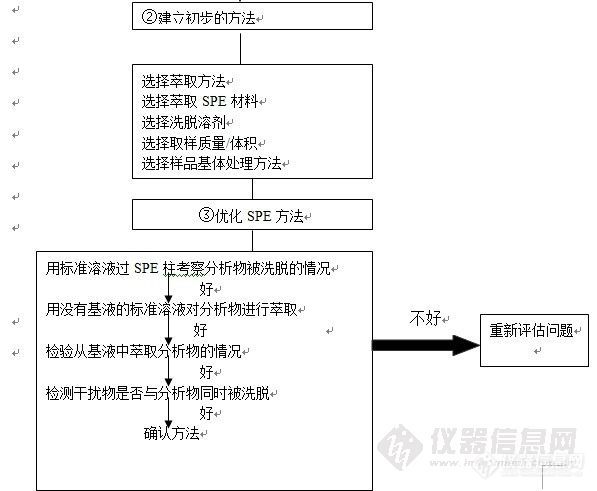
方法建立如下图片2.jpg:
![]() 1
1、初步固相萃取方法的建立
建立初步的萃取方法要考虑:
·选择合适的SPE柱
·选择合适的固相萃取方法
·方法的优化
2、固相萃取柱的选择<
1)柱填料的选择
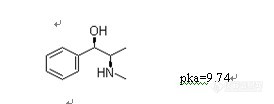
首选根据目标化合物与干扰物的差异,如极性,分子量,pka值等,选择合适的填料。
固相萃取柱的选择如下图片.jpg:
![]() 2)固相萃取柱规格的选择
2)固相萃取柱规格的选择对于反相、正相和吸附型固相萃取柱来说,被萃取样品的质量不超SPE柱填料的5%(参考值,同一种SPE柱对不同的目标物选择性不同,吸附容量不同);<P 0cm="0cm" 0cm? 0pt?>离子交换型的固相萃取柱,必须考虑离子交换的容量。不同厂家的小柱离子交换容量稍有差异。下表附SPE小柱的容量和洗脱参数
SPE柱上样容量和洗脱体积的选择
规格 | 最大上样量 | 最小洗脱体积 |
100mg/1mL | 5mg | 250µL |
200mg/3mL | 10mg | 500µL |
500mg/6mL | 25mg | 1.2mL |
1g/6mL | 50mg | 2.4mL |
3、选择合适的固相萃取方法
固相萃取的保留机制可分为两种:·吸附剂(填料)保留目标化合物:绝大多数化合物应用此机制,填料保留其目标组分及少量杂质,通过淋洗步骤去除吸附在柱上的少量杂质,最后选择合适的(洗脱)溶剂把目标组分洗脱下来。
根据吸附剂的保留机理可进一步分为:
(1)反相(C18,C8,CN,Phenyl,C4,C1)· 分析物:非极性至中等极性
· 基质:水溶性
· 方法:
a.活化:通常用水溶性有机溶剂如甲醇活化,然后用水平衡
b.淋洗:含0-50%极性溶剂的缓冲溶液淋洗杂质
c.洗脱:极性或非极性溶剂洗脱目标物
(2)正相(Silica, Florisil,Diol,NH2)·分析物:中等极性到强极性
· 基质:非极性至中等极性
· 方法:
a.活化:非极性有机溶剂b.洗脱:非极性有机溶剂如下图片:
![]() (3)阳离子交换(SCX,PRS,COOH)
(3)阳离子交换(SCX,PRS,COOH)u 分析物:阳离子(碱性)化合物
u 方法:
1.活化:用于非极性有机溶剂中的样品时,可用样品溶剂来活化;在用于极性溶剂中的样品时,可用水溶性有机溶剂过柱后,然后用水平衡,最后再用适当pH值的缓冲溶液进行平衡。
2.上样:样品溶液pH值要
小于其pKa两个单位(以保证其带电荷 )
3.洗脱:洗脱溶液pH值要
大于其pKa两个单位(中和分析物的电荷)
(4)阴离子交换(SAX,PSA,NH2,PAX/MAX )u 分析物:阴离子(酸性)化合物
u 方法:
1.活化:用于非极性有机溶剂中的样品时,可用样品溶剂来活化;在用于极性溶剂中的样品时,可用水溶性有机溶剂活化后,然后用水平衡,最后再用适当pH值的缓冲溶液进行平衡。
2.上样:样品溶液pH值要
大于其pKa两个单位(以保证其带电荷 )。
3.洗脱:洗脱溶液pH值要
小于其pKa两个单位(中和分析物的电荷)。
u 吸附剂(填料)保留杂质:
食品中色素等杂质的去除多用此机制。填料保留杂质而不保留或只保留极少量的目标组分,所以上样后即开始收集目标组分,最后用目标物所在的溶剂进一步洗脱。合并两部分收集液。
(1)活化:以样品所在的有机溶剂进化活化,1-2柱管体积
(2)上样:提取液转移至柱内,并收集流出液
(3)洗脱:用样品所在的有机溶剂进一步洗脱,收集流出液。合并上样和洗脱流出液。
4、固相萃取方法的优化
1)影响萃取效率的因素
(1)填料(固定相)----- 核心选择合适的SPE柱是保证理想结果的前提。
(2)洗脱溶剂的强度:Ø 采用正相固定相时,溶剂强度随其极性增强而增加;
Ø 采用反相固定相时,溶剂强度随极性减弱而增强。
(3)pH值: 离子交换固定相、被分析物和干扰物质的pKa各不相同。通过调节pH大小,可以使固定相带电荷,被分析物带相反电荷,而使干扰物质不带电荷;或者反过来,使固定相带电荷,干扰物质带相反电荷,而使被分析物不带电荷。
(4)操作:控制合适的流速、活化的时不要让柱干涸等
2)常见问题及解决方法·分析物回收率低
·萃取重现性差
·洗脱馏分中含有干扰物
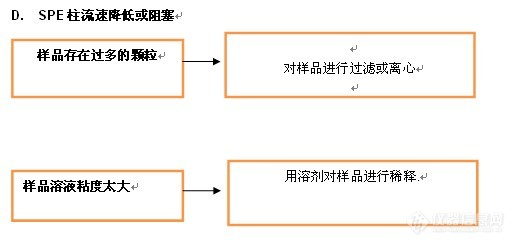
·SPE柱流速降低或阻塞
具体解决方案如下:
A.
分析物回收率低• 未保留?
• 被淋洗?
• 未被洗脱或部分洗脱?
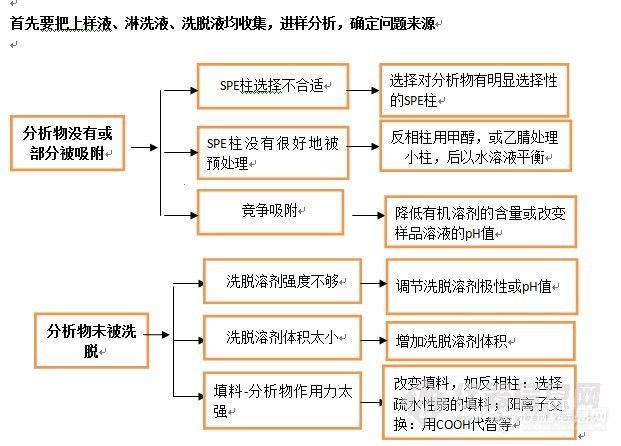
首先要把上样液、淋洗液、洗脱液均收集,进样分析,确定问题来源
回收率差如下图片 :
![]()
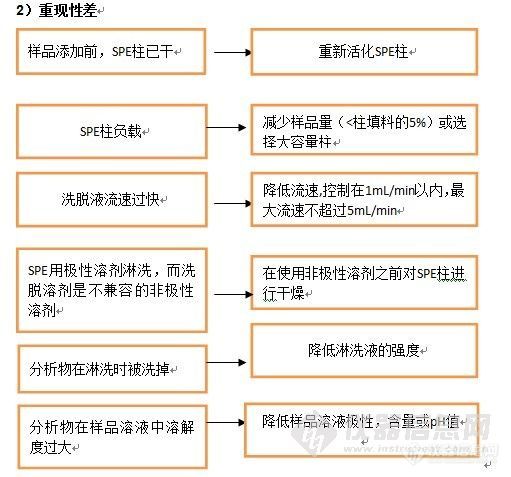
重现性差如下图片:
![]()
相关图片如下 :
![]()
相关图片如下:
![]() 举例说明1. 参考文献方法用C18柱做相关药物的净化,过柱方法如下:分别用乙酸乙酯、甲醇和水活化小柱,然后把处理过的样品过柱(溶剂为具一定pH值得缓冲溶液),水淋洗小柱后,用乙酸乙酯洗脱目标物。结果:接受液混浊状,回收率和重现性都不理想,可能是什么原因呢?答案:正确的做法是要在淋洗过程结束后把小柱完全抽干。原因有二,其一因为淋洗溶剂(水)与洗脱溶剂(乙酸乙酯)不互溶,如果不抽干洗脱溶剂与目标物不能充分作用,所以造成回收率和重现性都没有保证,同时从外观上看 接受液是液混浊液;其二如果淋洗过程不抽干小柱,洗脱溶剂里会引入水(淋洗剂),对下一步浓缩造成很大的困难。相关图片如下:
举例说明1. 参考文献方法用C18柱做相关药物的净化,过柱方法如下:分别用乙酸乙酯、甲醇和水活化小柱,然后把处理过的样品过柱(溶剂为具一定pH值得缓冲溶液),水淋洗小柱后,用乙酸乙酯洗脱目标物。结果:接受液混浊状,回收率和重现性都不理想,可能是什么原因呢?答案:正确的做法是要在淋洗过程结束后把小柱完全抽干。原因有二,其一因为淋洗溶剂(水)与洗脱溶剂(乙酸乙酯)不互溶,如果不抽干洗脱溶剂与目标物不能充分作用,所以造成回收率和重现性都没有保证,同时从外观上看 接受液是液混浊液;其二如果淋洗过程不抽干小柱,洗脱溶剂里会引入水(淋洗剂),对下一步浓缩造成很大的困难。相关图片如下:
![]() 2、
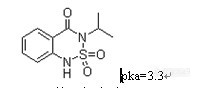
2、水中的灭草松前处理方法
取500ml水样过滤,待过Cleanert PEP柱(相当于Waters HLB)净化
1) 用5mL四氢呋喃洗柱子,除掉杂质
2) 用5mL甲醇1mL/min活化柱子
3) 用5mL纯水1mL/min活化柱
4) 500mL的水样以5mL/min的速度过柱
5) 5mL纯水2mL/min淋洗
6) 小柱真空抽干20min
7) 0.9mL的甲醇1mL/min淋洗,弃去淋洗液
8) 3mL四氢呋喃1mL/min的速度洗脱柱子,收集洗脱液浓缩定容至3mL
液相检测。
结果:回收率不理想,请问此方法有何问题?
答案:因为目标物灭草松呈酸性,pKa=3.3,而选择的小柱PEP是极性的。所以正确的做法是样品在过柱之前一定要调节水样的pH值小于等于3,使目标物分子化,以保证目标物能被小柱充分保留,否则在上柱的过程中容易造成“漏”的现象,从而造成回收率差。
三、固相技术应用实例解析
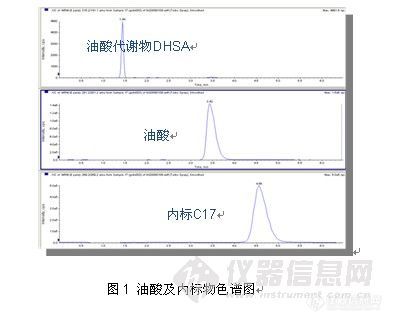
1、食品领域应用
1)动物组织中盐酸克仑特罗等4种β-激动剂药物残留检测(Cleanert PCX, P/N: CX1506)
1.实验材料1.1 固相萃取小柱:PCX(150mg/6mL)
1.2 四种β-激动剂药物:盐酸克仑特罗、沙丁胺醇、西马特罗、莱克多巴胺等4种β-激动剂药物。
2. 试样的制备取猪肝空白样品,经过液液萃取初步处理后,添加适宜浓度的标准溶液作为空白添加试样。
3. 净化 依次用甲醇5mL、水5mL和30mmol/L盐酸5mL润洗固相萃取小柱,将上述备用液过柱,依次用水5mL、甲醇5mL淋洗,真空抽干,用4%氨化甲醇5mL洗脱PCX小柱,收集洗脱液于具塞玻璃试管中,50℃下氮气吹干。在样液过柱和洗脱过程中流速控制在1mL/min左右。
4. 衍生化及检测将上述盛有残渣的具塞玻璃试管放入50℃烘箱中加热片刻,除去水分后,加入甲苯100mL和双三甲基硅基三氟乙酰胺(BSTFA)100mL,涡旋振荡20s,密封玻璃塞,置于80℃恒温烘箱中加热1小时,冷却后加入300mL甲苯,作为试样溶液,供
气相色谱-质谱分析(色谱柱:DA-5MS, 30m×0.25mm×0.25µm,P/N:1525-3002)。
5. 结果5.1 回收率实验(精密度和准确度)
将猪肝空白样品经过液液萃取初步处理后,分别添加一定量的标准溶液,配制1μg/L、2μg/L、5μg/L、10μg/L和100μg/L五个浓度的试样溶液,每批次内同一浓度做5次平行实验,共4个批次(样品典型回收率色谱图见附图)。
猪肝中实验结果列表如下
添加浓度 (μg/L) | 回收浓度 (μg/L) | 平均回收值 (μg/L) | 平均回收率 (%) | 相对标准偏差 (%) |
1 | 0.75 | 0.72 | 72.40 | 5.93 |
0.67 |
0.72 |
0.70 |
0.78 |
2 | 1.62 | 1.63 | 81.30 | 1.23 |
1.66 |
1.60 |
1.61 |
1.64 |
5 | 4.02 | 4.24 | 84.80 | 4.16 |
4.10 |
4.27 |
4.38 |
4.43 |
10 | 8.24 | 8.45 | 84.45 | 2.81 |
8.35 |
8.77 |
8.62 |
8.25 |
100 | 90.24 | 9.12 | 91.15 | 2.86 |
87.15 |
91.77 |
92.62 |
93.95 |
5.2重复性实验(批间误差实验):
猪肝中实验结果列表如下
批间 | 添加浓度(μg/L) |
1 | 2 | 5 | 10 | 100 |
平均 回收率% | RSD% | 平均 回收率% | RSD% | 平均 回收率% | RSD% | 平均 回收率% | RSD% | 平均 回收率% | RSD% |
1 | 72.40 | 5.93 | 81.30 | 3.49 | 84.80 | 6.16 | 84.45 | 3.59 | 91.15 | 2.86 |
2 | 75.37 | 6.12 | 80.47 | 5.37 | 84.74 | 7.55 | 87.46 | 4.68 | 90.05 | 3.86 |
3 | 70.09 | 7.85 | 80.80 | 6.57 | 83.10 | 8.17 | 83.21 | 5.39 | 89.53 | 4.16 |
4 | 76.73 | 4.90 | 78.50 | 8.35 | 82.90 | 5.11 | 85.95 | 5.72 | 88.27 | 5.93 |
平均值 | 73.65 | 6.20 | 80.25 | 5.95 | 83.88 | 6.75 | 85.27 | 4.84 | 89.75 | 4.20 |
RSD% | 12.95 | 10.79 | 9.43 | 7.00 | 5.75 |
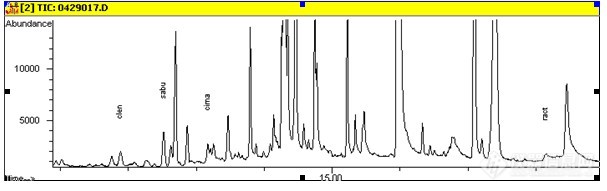
附图:猪肝中0.5μg/L、1μg/L、2μg/L、5μg/L、10μg/L和100μg/L六个浓度检测结果总离子流图(TIC)代表图谱:
猪肝+1ppb(PCX)
相关图片如下
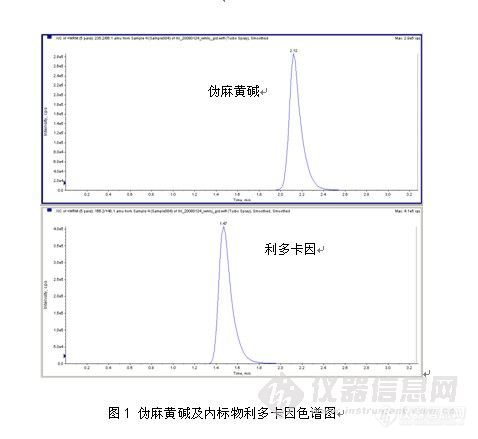
![]() 2)鸡蛋中三聚氰胺的检测(Cleanert PCX, P/N: CX0603)
2)鸡蛋中三聚氰胺的检测(Cleanert PCX, P/N: CX0603)
1 材料和方法
1.1 主要仪器和试剂,色谱柱(Venusil ASB C8,4.6*250mm,5μm,艾杰尔科技),混合型阳离子交换固相萃取柱(Cleanert PCX,60mg/3mL,艾杰尔科技),12位固相萃取装置(艾杰尔科技),高效
液相色谱仪;高速离心机;超声波震荡仪;涡旋混合器;分析天平(万分之一);溶剂过滤器(带0.45μm有机、水系过滤膜和真空泵);乙腈(HPLC级);三聚氰胺标准品(≥99.0%);柠檬酸(分析纯);庚烷磺酸钠(色谱级);水(二次蒸馏水以上)。
1.2 色谱条件:色谱柱:Venusil ASB C8,4.6*250mm,5μm;
流动相:乙腈∶10mM/L柠檬酸+10mM/L庚烷磺酸钠缓冲液=7∶93(pH=3.0)
检测波长:240nm;流速:1mL/min;进样20μL。
2 实验部分
2.1 三聚氰胺标准溶液配制:称取三聚氰胺标样10.0mg,加流动相溶解定容至100mL,即得浓度为100mg/L的三聚氰胺标样溶液。将浓度为100mg/L的三聚氰胺标准溶液分别用水稀释成浓度为1mg/L 、5mg/L 、10mg/L 、15mg/L 、20mg/L的标准品溶液,用0.45μm滤膜过滤后进
液相色谱检测。
2.2 1%三氯乙酸溶液溶液的配制称取三氯乙酸1.00g,加水溶解定容至1000mL即得。
2.3 5%氨化甲醇的配制准确量取5mL氨水和95mL甲醇,混匀后备用。
2.4 5%醋酸铅溶液的配制称取5.0g醋酸铅,加水溶解定容至100mL即得。
2.5 混合型阳离子交换固相萃取柱(Cleanert PCX 60mg/3mL)的活化取Cleanert PCX 固相萃取柱,以3mL甲醇,3mL水依次过柱活化,弃去流出液,备用。
2.5 加标样本处理将鸡蛋打开搅匀,分别称取1.00g鸡蛋样本置于10mL具塞离心管中,分别加入100mg/L三聚氰胺标样溶液10μl、20μl、100μl,分别得到添加浓度为1.0mg/kg、2.0mg/kg、10.0mg/kg的样本。
往装有上述样本的具塞离心管中分别加入10mL 1%三氯乙酸溶液,2mL 5%醋酸铅溶液,摇匀,超声20分钟,8000rpm离心10分钟,全部上清液转入活化好的混合型阳离子交换固相萃取柱(Cleanert PCX,60mg/3mL),依次使用3mL水,3mL甲醇淋洗,抽干,弃去淋洗液。最后用5mL 5%的氨化甲醇洗脱(V/V),接收洗脱液,50℃氮气吹干,用1mL流动相定容,0.45μm滤膜过滤后进
液相色谱检测。
另取空白鸡蛋样本1.00g,不添加三聚氰胺照上述方法处理,作为空白对照样品。
3实验结果:
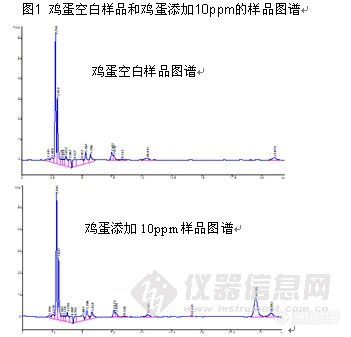
3.1 峰型与分离度图片如下
![]()
由图1可见,用该方法处理,三聚氰胺峰型对称尖锐,且与杂质分离良好
3.2 精密度分别移取浓度为1.0mg/L、5.0mg/L的三聚氰胺标准溶液,分别连续进样6次,结果如表1所示。
表1 保留时间与峰面积的稳定性数据
浓度mg/mL | 指标 | 1# | 2# | 3# | 4# | 5# | 6# | 平均值 | RSD% |
1.0 | 保留时间(min) | 18.830 | 18.829 | 18.829 | 18.838 | 18.840 | 18.834 | 18.833 | 0.026 |
峰面积 | 89 | 81 | 84 | 88 | 84 | 80 | 84 | 4.286 |
5.0 | 保留时间(min) | 18.949 | 18.952 | 18.947 | 18.949 | 18.950 | 18.946 | 18.949 | 0.011 |
峰面积 | 423 | 440 | 438 | 439 | 437 | 438 | 436 | 1.461 |
由表1结果可见,本方法具有很好的精密度和重现性。
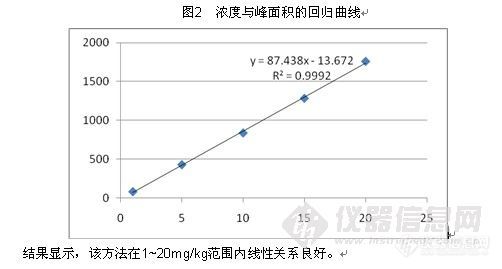
3.3 标准校正曲线表2 标准校正曲线实验数据
浓度 mg/kg | 峰面积
第1次进样 | 峰面积
第2次进样 | 峰面积 均值 |
1.0 | 89 | 79 | 84 |
5.0 | 423 | 440 | 431 |
10.0 | 832 | 844 | 838 |
15.0 | 1265 | 1299 | 1282 |
20.0 | 1689 | 1823 | 1756 |
根据以上数据计算线性方程为:y = 87.43x - 13.67, R² = 0.999 ,相关曲线见图2。
![]()
3.4 添加回收率
表3 添加浓度与回收率数据
添加浓度(mg/kg) | 峰面积 | 计算含量 | 回收率(%) |
1.0 | 19.9 | 1.158892 | 115.89 |
1.0 | 21.0 | 1.214532 | 121.45 |
2.0 | 41.7 | 2.261587 | 113.08 |
2.0 | 40.8 | 2.216062 | 110.80 |
10.0 | 188.8 | 9.702247 | 97.02 |
10.0 | 219.6 | 11.26018 | 112.60 |
由表3可见,本方法检测鸡蛋中三聚氰胺回收率较好。
4 结论通过上述实验可见,运用本方法测定鸡蛋中三聚氰胺,基质净化效果好,杂质干扰小,色谱峰型良好对称度高,操作简单方便,和准确度高等优点,非常适用于鸡蛋中三聚氰胺的检测。