维权声明:本文为sally0326原创作品,本作者与仪器信息网是该作品合法使用者,该作品暂不对外授权转载。其他任何网站、组织、单位或个人等将该作品在本站以外的任何媒体任何形式出现均属侵权违法行为,我们将追究法律责任。
因为总要做样品制备,需要寻找合适的C18填料来进行分离,所以前期HPLC分析和后期的Flash制备C18,一般不是一个型号,在此过程中出现一个很奇怪的现象,大家来分析下原因呗:
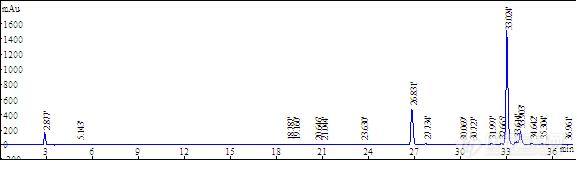
同一个样品,有制备色谱和分析做不出来的谱图如下,色谱条件都一样,可是出峰顺序尽然颠倒了,为什么呢??同志们有遇到过么?
流动相:B ——乙腈
A ——0.01mol/L 磷酸二氢钾水溶液 PH值=3.3
分析柱:
Venusil XBP C18 5μm 100Å 4.6*250mm制备柱:
Venusil MP C18 5μm 100Å 21.2*250mm![]() 样品分析
样品分析
![]()
局部放大
![]()
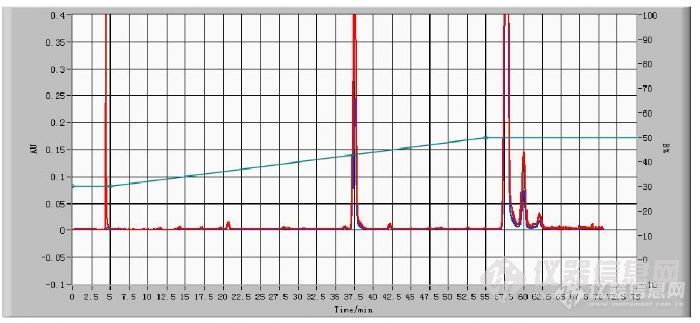
制备谱图
个人觉得,这是不是因为填料选择性不同导致的呢?选择性不同,应该只会导致分离度不同啊,不应该说出峰顺序不同的呢。
觉得可能得原因如下,不是很确定,还请各位高手讨论:
1、填料选择性不同
2、上样量导致
网上搜索了下反相色谱原理,如下:
使用将特定的液态物质涂于担体表面,或化学键合于担体表面而形成的固定相,分离原理是根据被分离的组分在流动相和固定相中溶解度不同而分离。分离过程是一个分配平衡过程。
反相色谱法 一般用非极性固定相(如C18、C8);流动相为水或缓冲液,常加入甲醇、乙腈、异丙醇、丙酮、四氢呋喃等与水互溶的有机溶剂以调节保留时间。适用于分离非极性和极性较弱的化合物。
出峰顺序,极性大的先出峰,极性小的后出峰。
个人觉得,反相色谱的作用机理相对比较复杂,一般有如下几条:
1、疏水作用
即常规的反相作用机理,出峰顺序是极性大的先出,极性小的后出峰
2、氢键作用
主要看化合物结构式是否能形成氢键。氢键作用力越大,出峰越晚
3、离子交换
反相C18是在硅胶基质上键合十八烷基形成的,因此硅胶上面还是有酸性。
4、金属螯合作用
没有百分百纯度的固定相,里面多多少少还是会含有一部分金属离子,而金属离子在和化合物作用过程中,会产生螯合,导致出峰变慢。
因此出峰的先后,并不是单纯的看化合物的极性,不同的C18,对某一化合物的作用是不同的。所以在做分离的时候,为了避免重复工作,建议分析和分离用同一款C18会比较好。